题目内容
下列离子方程式正确的是( )
| A、FeI2溶液中通入过量Cl2:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
| B、已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O═2HClO+CO32- |
| C、向含有硫酸钙的水垢中加入碳酸钠溶液:CaSO4+CO32-═CaCO3+SO42- |
| D、Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氯气过量,碘离子、亚铁离子都完全被氯气氧化,碘离子的计量数错误;
B.次氯酸的酸性大于碳酸氢根离子,次氯酸钠与二氧化碳反应生成的是碳酸氢根离子;
C.碳酸钙的溶解度小于硫酸钙,硫酸钙与碳酸根离子反应生成更难溶的碳酸钙;
D.根据质量守恒判断,该离子方程式两边氧原子数目不相等.
B.次氯酸的酸性大于碳酸氢根离子,次氯酸钠与二氧化碳反应生成的是碳酸氢根离子;
C.碳酸钙的溶解度小于硫酸钙,硫酸钙与碳酸根离子反应生成更难溶的碳酸钙;
D.根据质量守恒判断,该离子方程式两边氧原子数目不相等.
解答:
解:A.FeI2溶液中通入过量Cl2,亚铁离子、碘离子都完全被氯气氧化,反应的离子方程式为:2Fe2++4I-+3Cl2═2Fe3++2I2+6Cl-,故A错误;
B.根据电离平衡常数H2CO3>HClO>HCO3-可知,碳酸钠与二氧化碳反应生成碳酸氢根离子,正确的离子方程式为:ClO-+CO2+H2O═HClO+HCO3-,故B错误;
C.向含有硫酸钙的水垢中加入碳酸钠溶液,碳酸钙比硫酸钙更难溶,实现了沉淀转化,反应的离子方程式为:CaSO4+CO32-═CaCO3+SO42-,故C正确;
D.Na2O2与H2O反应生成氢氧化钠和氧气,正确的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑,故D错误;
故选C.
B.根据电离平衡常数H2CO3>HClO>HCO3-可知,碳酸钠与二氧化碳反应生成碳酸氢根离子,正确的离子方程式为:ClO-+CO2+H2O═HClO+HCO3-,故B错误;
C.向含有硫酸钙的水垢中加入碳酸钠溶液,碳酸钙比硫酸钙更难溶,实现了沉淀转化,反应的离子方程式为:CaSO4+CO32-═CaCO3+SO42-,故C正确;
D.Na2O2与H2O反应生成氢氧化钠和氧气,正确的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑,故D错误;
故选C.
点评:本题考查了离子方程式的正误判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
 2013年,全国出现多例人感染H7N9禽流感病毒,达菲(化学名:磷酸奥司他韦)一度受到人们的关注.如图为达菲的结构简式,下列说法不正确的是( )
2013年,全国出现多例人感染H7N9禽流感病毒,达菲(化学名:磷酸奥司他韦)一度受到人们的关注.如图为达菲的结构简式,下列说法不正确的是( )| A、可以用红外光谱仪测定达菲的某些官能团 |
| B、达菲的化学式为:C16H28N2O4?H3PO4 |
| C、达菲在一定条件下能与NaOH溶液反应 |
| D、达菲能与FeCl3溶液反应显紫色 |
下列化学用语书写正确的是( )
A、CH4分子的比例模型: |
B、氯原子的结构示意图: |
C、NH3分子的电子式: |
| D、CS2结构式:S=C=S |
下列说法错误的是( )
| A、PM2.5又称细颗粒物,是指空气动力学当量直径小于等于2.5微米的颗粒物.因其粒径小,面积大,活性强,易附带有毒、有害物质(例如,重金属、微生物等),对人体健康和大气环境质量的影响更大 |
| B、“水滴石穿”主要是溶解了CO2的雨水与CaCO3长期作用,生成了可溶性的Ca(HCO3)2 |
| C、食品安全已成为各地政府和公众关注的热点话题,严禁向食品中添加任何非食用物质和滥用食品添加剂 |
| D、一氧化碳有毒,生有煤炉的居室,可放置数盆水,这样可有效地吸收一氧化碳,以防煤气中毒 |
常温下,0.2mol?L-1的盐酸30mL分别与下列Na2CO3溶液混合,再加水稀释到100mL,其中最初产生CO2的速率最快的是( )
| A、20mL 0.3mol?L-1 Na2CO3 |
| B、10mL 0.4mol?L-1 Na2CO3 |
| C、25mL 0.4mol?L-1 Na2CO3 |
| D、15mL 0.5mol?L-1 Na2CO3 |
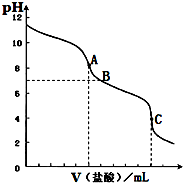 用0.1000mol?L-1的盐酸滴定10.00mL 0.1000mol?L-1的碳酸钠溶液,溶液pH值与加入盐酸的体积的关系如图所示.已知室温时饱和CO2的pH为3.9,0.05mol?L-1 NaHCO3的pH约为8.3.下列叙述中不正确的是( )
用0.1000mol?L-1的盐酸滴定10.00mL 0.1000mol?L-1的碳酸钠溶液,溶液pH值与加入盐酸的体积的关系如图所示.已知室温时饱和CO2的pH为3.9,0.05mol?L-1 NaHCO3的pH约为8.3.下列叙述中不正确的是( )| A、以酚酞为指示剂,溶液颜色突变时(A点),Na2CO3转化为NaHCO3 |
| B、以甲基橙为指示剂,当溶液颜色突变时,共消耗盐酸20.00mL |
| C、溶液pH=7时(B点),Na2CO3完全转化为NaCl |
| D、BC段对应溶液中CO2与NaHCO3共存 |
O、Si、Al是地壳中含量最多的三种元素,Na、Mg、Cl是海水中的重要元素.下列说法正确的是( )
| A、普通玻璃、水泥成分中都含有O、Si、Al三种元素 |
| B、从海水中制备Na、Mg、Al三种元素单质的反应都是氧化还原反应 |
| C、电解熔融状态的SiO2、Al2O3可以制得Si、Al,且都有氧气生成 |
| D、加热蒸干NaCl、MgCl2溶液时可以得到晶体NaCl、MgCl2 |

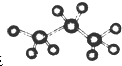
 与C8H6互为同分异构体.
与C8H6互为同分异构体.