题目内容
取混有NaCl的Na2CO3固体20.0g溶于水配成100mL溶液,取出20.00mL于锥形瓶中,向锥形瓶中逐滴滴入某浓度的盐酸直至没有气体放出为止,用去盐酸15.00mL,并收集到672mL CO2(标准状况).试计算:
(1)所用盐酸的物质的量浓度
(2)Na2CO3的质量分数.
(1)所用盐酸的物质的量浓度
(2)Na2CO3的质量分数.
考点:化学方程式的有关计算
专题:计算题
分析:混合物与盐酸发生反应:Na2CO3+2HCl═2NaCl+CO2↑+H2O,根据n=
计算反应生成的二氧化碳的物质的量,根据二氧化碳的物质的量反应的化学方程式计算相关物理量.
| V |
| Vm |
解答:
解:n(CO2)=
=
=0.03mol
Na2CO3 +2HCl═2NaCl+CO2↑+H2O
106g 2mol 1mol
m(Na2CO3) n(HCl) 0.03mol
(1)n(HCl)=2×n(CO2)=0.06mol;
c(HCl)=
=
=4.0mol/L,
答:所用盐酸的物质的量浓度为4.0mol/L;
(2)m(Na2CO3)=
=3.18g,
因取混有NaCl的Na2CO3固体20.0g溶于水配成100mL溶液,取出20.00mL于锥形瓶中,所以100mL溶液中碳酸钠为3.18g的5倍,Na2CO3的质量分数=
×100%=79.5%,
答:Na2CO3的质量分数为79.5%.
| V |
| Vm |
| 0.672L |
| 22.4mol/L |
Na2CO3 +2HCl═2NaCl+CO2↑+H2O
106g 2mol 1mol
m(Na2CO3) n(HCl) 0.03mol
(1)n(HCl)=2×n(CO2)=0.06mol;
c(HCl)=
| n |
| v |
| 0.06mol |
| 0.0015L |
答:所用盐酸的物质的量浓度为4.0mol/L;
(2)m(Na2CO3)=
| 106g/mol×0.03mol |
| 1mol |
因取混有NaCl的Na2CO3固体20.0g溶于水配成100mL溶液,取出20.00mL于锥形瓶中,所以100mL溶液中碳酸钠为3.18g的5倍,Na2CO3的质量分数=
| 3.18g×5 |
| 20g |
答:Na2CO3的质量分数为79.5%.
点评:本题考查混合物的有关计算,清楚发生的反应时解题关键,题目难度中等,注意根据方程式进行解答.

练习册系列答案
相关题目
Mg、Al 两者组成的混合物与足量盐酸反应,产生 H2在标准状况下的体积是4.48L,下列推断中不正确的是( )
| A、参加反应的Mg、Al 两者共0.2 mol. |
| B、参加反应的HCl 共0.4 mol. |
| C、Mg、Al在反应中共失去0.4 mol电子 |
| D、若与足量稀硫酸反应产生H20.2 mol |
某无色溶液加入氯化钡溶液后有白色沉淀,再加稀硝酸沉淀不消失,则该溶液中( )
| A、一定含有SO42- |
| B、一定含有Ag+ |
| C、可能含有SO42-或 SO32- 或Ag+ |
| D、一定含有Ag+、SO42 |
下列实验操作中,所用仪器合理的是( )
| A、分离四氯化碳和水的混合物用分液漏斗 |
| B、用100 mL的量筒量取5.2 mL的盐酸 |
| C、用托盘天平称取25.20g NaCl |
| D、用100 mL容量瓶配制50 mL 0.1 mol/L的盐酸 |
用向下排空气法收集的气体是( )
| A、HCl |
| B、NH3 |
| C、NO |
| D、C12 |
 实验室某些物质的制备装置如图所示(省略夹持装置和净化装置),仅用此装置和表中提供的物质完成相关实验,最合理的是( )
实验室某些物质的制备装置如图所示(省略夹持装置和净化装置),仅用此装置和表中提供的物质完成相关实验,最合理的是( )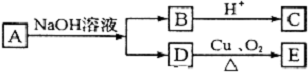 某有机物A的分子式为C6H12O2,已知A~E有如图转化关系,且D不与Na2CO3溶液反应,C、E均能发生银镜反应,则A的结构可能有( )
某有机物A的分子式为C6H12O2,已知A~E有如图转化关系,且D不与Na2CO3溶液反应,C、E均能发生银镜反应,则A的结构可能有( )