题目内容
高铁酸钾是一种高效的多功能的水处理剂.工业上常采用NaClO氧化法生产,原理为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O Na2FeO4+2KOH=K2FeO4+2NaOH主要的生产流程如下:

(1)写出反应①的离子方程式 .
(2)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响.
图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响.

工业生产中最佳温度为 ℃,此时Fe(NO3)3与NaClO两种溶液最佳质量浓度之比为 .
(3)“提纯”K2FeO4中所包含的操作依次为:溶解、 、过滤、洗涤、低温干燥,其中K2FeO4在水溶液中易水解:4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2↑.则洗涤剂最好选用 溶液(填序号).
A.H2O B.CH3COONa、异丙醇C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(4)上述方法是湿法制备高铁酸钾,干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,每生成1molNa2FeO4转移 mol电子.
(5)我国学者提出在浓NaOH溶液(非饱和溶液)中用电化学方法来制备高铁酸盐,电解装置如图3.电解时,阳极的电极式反应为 .

(1)写出反应①的离子方程式
(2)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响.
图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响.

工业生产中最佳温度为
(3)“提纯”K2FeO4中所包含的操作依次为:溶解、
A.H2O B.CH3COONa、异丙醇C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(4)上述方法是湿法制备高铁酸钾,干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,每生成1molNa2FeO4转移
(5)我国学者提出在浓NaOH溶液(非饱和溶液)中用电化学方法来制备高铁酸盐,电解装置如图3.电解时,阳极的电极式反应为
考点:制备实验方案的设计,物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:向NaOH溶液中通入Cl2,发生的反应为Cl2+2NaOH=NaCl+NaClO+H2O,然后向溶液中加入Fe(NO3)3,发生的反应为3NaClO+2 Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O,向溶液中加入HCl来调节溶液的pH,然后过滤得到NaCl,向滤液中加入饱和KOH,发生反应Na2FeO4+2KOH=K2FeO4+2NaOH,分离得到粗的K2FeO4,通过提纯得到纯的K2FeO4,
(1)由工艺流程可知,反应①为氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水;
(2)Fe(NO3)3浓度一定,K2FeO4的生成率最高时的温度为最佳温度;
由图1可知,Fe(NO3)3浓度在375g/L时,K2FeO4的生成率最高,由图2可知,NaClO在255g/L时,K2FeO4的生成率最高,据此计算Fe(NO3)3与NaClO两种溶液最佳质量浓度之比;
(3)K2FeO4 在水溶液中易水解呈碱性,应选择碱性非水溶液抑制K2FeO4水解,进行洗涤;
(4)2FeSO4+6Na2O2═2NaFeO4+2Na2O+2Na2SO4+O2↑中Fe、O元素的化合价升高,O元素的化合价降低,由化合价的变化计算转移的电子数;
(5)电解时阳极发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O.
(1)由工艺流程可知,反应①为氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水;
(2)Fe(NO3)3浓度一定,K2FeO4的生成率最高时的温度为最佳温度;
由图1可知,Fe(NO3)3浓度在375g/L时,K2FeO4的生成率最高,由图2可知,NaClO在255g/L时,K2FeO4的生成率最高,据此计算Fe(NO3)3与NaClO两种溶液最佳质量浓度之比;
(3)K2FeO4 在水溶液中易水解呈碱性,应选择碱性非水溶液抑制K2FeO4水解,进行洗涤;
(4)2FeSO4+6Na2O2═2NaFeO4+2Na2O+2Na2SO4+O2↑中Fe、O元素的化合价升高,O元素的化合价降低,由化合价的变化计算转移的电子数;
(5)电解时阳极发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O.
解答:
解:向NaOH溶液中通入Cl2,发生的反应为Cl2+2NaOH=NaCl+NaClO+H2O,然后向溶液中加入Fe(NO3)3,发生的反应为3NaClO+2 Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O,向溶液中加入HCl来调节溶液的pH,然后过滤得到NaCl,向滤液中加入饱和KOH,发生反应Na2FeO4+2KOH=K2FeO4+2NaOH,分离得到粗的K2FeO4,通过提纯得到纯的K2FeO4,
(1)反应①为氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水,反应离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(2)由图1可知,Fe(NO3)3浓度一定,温度在26℃时,K2FeO4的生成率最高,故工业生产中最佳温度为26℃.
由图1可知,Fe(NO3)3浓度在330g/L时,K2FeO4的生成率最高,由图2可知,NaClO在2575g/L时,K2FeO4的生成率最高,所以Fe(NO3)3与NaClO两种溶液最佳质量浓度之比为330g/L:275g/L=6:5,
故答案为:26;6:5;
(3)提纯”K2FeO4中所包含的操作依次为:溶解、蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥,K2FeO4 在水溶液中易水解呈碱性,应选择碱性非水溶液抑制K2FeO4水解,进行洗涤.
A.H2O,不能抑制水解,且容易损失,故A错误;
B.CH3COONa、异丙醇,能抑制水解,减少洗涤损失,故B正确;
C.NH4Cl、异丙醇,不能抑制水解,促进水解,故C错误;
D.Fe(NO3)3、异丙醇,不能抑制水解,促进水解,故D错误.
故答案为:蒸发浓缩、冷却结晶;B;
(4)反应中Fe元素化合价由+2价升高为+6价,被氧化,过氧化钠中O元素的化合价由-1价降低为-2价,由-1价升高为0,由方程式可知,镁生成2molNa2FeO4,有6molNa2O2参加反应,转移10mol电子,则每生成1molNa2FeO4转移的电子数为5mol,
故答案为:5;
(5)电解时阳极发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O,故答案为:Fe+8OH--6e-═FeO42-+4H2O.
(1)反应①为氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水,反应离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(2)由图1可知,Fe(NO3)3浓度一定,温度在26℃时,K2FeO4的生成率最高,故工业生产中最佳温度为26℃.
由图1可知,Fe(NO3)3浓度在330g/L时,K2FeO4的生成率最高,由图2可知,NaClO在2575g/L时,K2FeO4的生成率最高,所以Fe(NO3)3与NaClO两种溶液最佳质量浓度之比为330g/L:275g/L=6:5,
故答案为:26;6:5;
(3)提纯”K2FeO4中所包含的操作依次为:溶解、蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥,K2FeO4 在水溶液中易水解呈碱性,应选择碱性非水溶液抑制K2FeO4水解,进行洗涤.
A.H2O,不能抑制水解,且容易损失,故A错误;
B.CH3COONa、异丙醇,能抑制水解,减少洗涤损失,故B正确;
C.NH4Cl、异丙醇,不能抑制水解,促进水解,故C错误;
D.Fe(NO3)3、异丙醇,不能抑制水解,促进水解,故D错误.
故答案为:蒸发浓缩、冷却结晶;B;
(4)反应中Fe元素化合价由+2价升高为+6价,被氧化,过氧化钠中O元素的化合价由-1价降低为-2价,由-1价升高为0,由方程式可知,镁生成2molNa2FeO4,有6molNa2O2参加反应,转移10mol电子,则每生成1molNa2FeO4转移的电子数为5mol,
故答案为:5;
(5)电解时阳极发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O,故答案为:Fe+8OH--6e-═FeO42-+4H2O.
点评:本题考查学生对工艺流程的理解、阅读题目获取信息能力、物质的分离提纯等基本操作、氧化还原反应、电解池等,难度中等,需要学生具有扎实的基础知识及灵活运用知识、题目信息解决问题的能力.

练习册系列答案
相关题目
下列物质性质与应用的因果关系正确的是( )
| A、焦炭具有强还原性,高温下能将二氧化硅还原为硅 |
| B、晶体硅用于制作半导体材料是因其熔点高、硬度大 |
| C、二氧化锰具有强氧化性,故能将双氧水氧化为氧气 |
| D、Fe比Cu活泼,所以FeCl3溶液可以腐蚀线路板上的Cu |
以“创新?未来”为主题的第十四届上海国际车展在浦东新国际博览中心举行.车展期间,新一代电动汽车因其“技术含量高”“节能环保”而倍受关注.液态锂离子电池是一种被采用的车载电池,该电池的电极反应如下:正极6C+xLi++x e-═LixC6,负极LiNiO2-xe-═Li1-xNiO2+xLi+.则下列说法中正确的是( )
| A、放电时,电子从正极流向电源的负极 | |||
| B、放电时,Li+向负极移动 | |||
C、该电池的总反应为LiNiO2+6C
| |||
| D、充电时,阳极发生的电极反应为Li1-xNiO2+xLi++x e-═LiNiO2 |
下列装置的线路接通后,经过一段时间,溶液的pH值明显下降的是( )
A、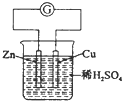 |
B、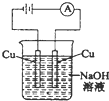 |
C、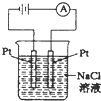 |
D、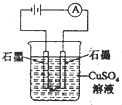 |
即使石蕊试液最终变为红色,又能使品红试液变为无色,还能使溴水褪色的是( )
| A、Cl2 |
| B、CO2 |
| C、SO2 |
| D、CO |
下列除杂质的方法正确的是( )
| A、用过量的碱液除去CO2中混有的少量HCl气体 |
| B、用饱和食盐水除去氯气中混有的HCl气体 |
| C、用升华的方法除去食盐中少量的I2 |
| D、用过量的氯化钡溶液除去亚硫酸钠溶液中的少量SO42- |
 完成下列热化学方程式(化学方程式、电极反应式、表达式等)的书写:
完成下列热化学方程式(化学方程式、电极反应式、表达式等)的书写:



 这一途径外,另一途径生成的中间产物的结构简式为
这一途径外,另一途径生成的中间产物的结构简式为