题目内容
【题目】下列物质一定属于同系物的是( ) ① ![]() ②
② ![]() ③
③ ![]() ④C2H4 ⑤CH2=CH﹣CH=CH2⑥C2H6⑦
④C2H4 ⑤CH2=CH﹣CH=CH2⑥C2H6⑦  ⑧
⑧ 
A.④和⑧
B.①、②和③
C.⑤、⑦和⑧
D.⑥和⑧
【答案】A
【解析】解:A.④和⑧均为烯烃,均只有一个碳碳双键,分子组成相差2个CH2原子团,为同系物,故A选; B.①、②和③的结构不相似,不是同系物,故B不选;
C.⑤、⑦中含2个碳碳双键,⑧中含1个碳碳双键,不是同系物,故C不选;
D.⑥为烷烃,⑧为烯烃,不是同系物,故D不选;
故选A.
【考点精析】通过灵活运用芳香烃、烃基和同系物,掌握分子里含有一个或多个苯环的碳氢化合物,称为芳香烃,其中由一个苯环和饱和烃基组成的芳香烃叫苯的同系物,其通式为CnH2n–6(n≥6)即可以解答此题.

【题目】MnSO4在工业中有重要应用.用软锰矿浆(主要成分为MnO2和水,含有Fe2O3、FeO、Al2O3和少量PbO等杂质)浸出制备MnSO4 , 其过程如下: I. 向软锰矿浆中通入SO2 , 锰、铁、铝、铅元素以离子形式浸出,测得浸出液的pH<2.
II. 向浸出液中加MnO2 , 充分反应后,加入石灰乳,调溶液pH=4.7.
III.再加入阳离子吸附剂,静置后过滤.
IV.滤液蒸发浓缩,冷却结晶,获得MnSO4晶体.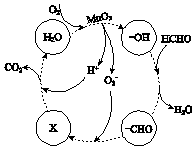
【资料】部分阳离子形成氢氧化物沉淀的pH
离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ | Pb2+ |
开始沉淀时的pH | 7.6 | 2.7 | 3.8 | 8.3 | 8.0 |
完全沉淀时的pH | 9.7 | 3.7 | 4.7 | 9.8 | 8.8 |
(1)I中向软锰矿浆中通入SO2生成MnSO4 , 该反应的化学方程式是 .
(2)II 中加入MnO2的主要目的是;调溶液 pH=4.7,生成的沉淀主要含有 和少量CaSO4 .
(3)III中加入阳离子吸附剂,主要除去的离子是 .
(4)用惰性电极电解MnSO4溶液,可以制得高活性MnO2 . ①电解MnSO4溶液的离子方程式是
②高活性MnO2可用于催化降解甲醛,有关微粒的变化如图所示,其中X是 , 总反应的化学方程式是 .