题目内容
1. (1)COC12俗称光气,分子中C原子采取sp2杂化成键,光气分子的结构式为
(1)COC12俗称光气,分子中C原子采取sp2杂化成键,光气分子的结构式为 ,其中碳氧原子之间共价键是c(填序号).
,其中碳氧原子之间共价键是c(填序号).a.2个σ键 b.2个π键 c.1个σ键,1个π键
(2)CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为
 .
.(3)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为4,δ、α两种晶胞中铁原子的配位数之比为4:3;在δ晶胞中空间利用率为68%,与其具有相同堆积方式的金属还有Na、K(填元素符号).
分析 (1)COCl2俗称光气,分子中C原子采取sp2杂化成键,C原子与氯原子之间形成C-Cl单键,故C原子与O原子之间形成C=O双键,双键中含有1个σ键、1个π键;
(2)等电子体的结构相似,故O22+的电子式与C22-的电子式相似,含有2个π键;
(3)利用均摊法计算;根据Fe原子周围O原子数判断;δ晶体晶胞的堆积方式为体心立方,据此分析.
解答 解:(1)COCl2俗称光气,分子中C原子采取sp2杂化成键,C原子与氯原子之间形成C-Cl单键,故C原子与O原子之间形成C=O双键,光气分子的结构式是 ,C=O双键中含有1个σ键、1个π键,
,C=O双键中含有1个σ键、1个π键,
故答案为: ;c;
;c;
(2)根据等电子体的结构相似,O22+的电子式与C22-的电子式相似,含有2个π键,O22+的电子式  ,
,
故答案为: ;
;
(3)γ晶体晶胞中所含有的铁原子数为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,δ、α两种晶胞中铁原子的配位数分别为8、6,则配位数之比为8:6=4:3,δ晶胞为体心立方堆积,空间利用率为:68%,与Na、K、具有相同堆积方式,
故答案为:4;4:3;68%;Na、K.
点评 本题主要考查核外电子排布规律、等电子体、化学键与晶胞结构、晶胞的计算等,侧重于考查学生对基础知识的综合应用能力,题目难度中等.

练习册系列答案
相关题目
11.已知: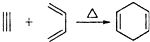 ,如果要合成
,如果要合成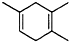 所用的原始原料可以是( )
所用的原始原料可以是( )
①2-甲基-1,3-丁二烯和2-丁炔 ②1,3-戊二烯和2-丁炔
③2,3-二甲基-1,3-戊二烯和乙炔 ④2,3-二甲基-1,3-丁二烯和丙炔.
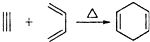 ,如果要合成
,如果要合成 所用的原始原料可以是( )
所用的原始原料可以是( )①2-甲基-1,3-丁二烯和2-丁炔 ②1,3-戊二烯和2-丁炔
③2,3-二甲基-1,3-戊二烯和乙炔 ④2,3-二甲基-1,3-丁二烯和丙炔.
| A. | 只有① | B. | ②③ | C. | ②④ | D. | ①④ |
12.室温下进行的下列实验,不能达到预期目的是( )
| 序号 | 实验内容 | 实验目的 |
| A | 在滴有酚酞的Na2CO3溶液中,滴加入BaC12溶液,溶液红色逐渐褪去 | 证明Na2CO3溶液中存在水解平衡 |
| B | 将Al泊插入浓硝酸中,无现象 | 证明Al和浓硝酸不反应 |
| C | 将两个完全相同且充满NO2的密闭烧瓶,分别浸泡于热水、冰水中 | 探究温度对化学平衡状态的影响 |
| D | 向同体积同浓度的H2O2溶液中,分别加入1mL同浓度的CuSO4、FeCl3溶液 | 比较Cu2+、Fe3+对H2O2分解速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
6.下列有机物中同分异构体数目最多的是( )
| A. | C8H10(芳香烃) | B. | 戊酸 | C. | C4H8Cl2 | D. | C4H8O2(酯) |
13.某化学兴趣小组利用废弃铝矿(含CuO、Al2O3及SiO2),模拟工业上提取铝的工艺,设计如图所示的简单操作流程:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)滤渣主要成分的化学式为Cu、Fe、SiO2.
(2)灼烧Al(OH)3时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有坩埚(填仪器名称).
(3)溶液Y中要加入稍过量原料A,原料A的化学式是NH3•H2O.
(4)操作流程中③的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(5)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,其原理如下图所示:

请写出该电池正极反应式Ag2O+2e-+H2O=2Ag+2OH-.

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | AlOH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)滤渣主要成分的化学式为Cu、Fe、SiO2.
(2)灼烧Al(OH)3时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有坩埚(填仪器名称).
(3)溶液Y中要加入稍过量原料A,原料A的化学式是NH3•H2O.
(4)操作流程中③的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(5)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,其原理如下图所示:

请写出该电池正极反应式Ag2O+2e-+H2O=2Ag+2OH-.
10.下列叙述正确的是( )
| A. | 溶液和胶体的本质区别是有无丁达尔效应 | |
| B. | 玻璃、水泥和光导纤维的主要成分都是硅酸盐 | |
| C. | 氧化钠和过氧化氢含有的化学键种类不同 | |
| D. | 常用的危险化学品酒精和甲烷的标志都是易燃液体 |
11.下列陈述中,Ⅰ、Ⅱ都正确且两者间具有因果关系的一组是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | Na2O2使酚酞溶液变红 | Na2O2能漂白织物、纸浆 |
| B | SO2可使石蕊溶液先变红后褪色 | SO2的水溶液具有酸性和漂白性 |
| C | NH3、HCl可用作喷泉实验 | NH3、HCl都极易溶于水 |
| D | 浓H2SO4有吸水性 | 浓H2SO4可用于干燥氨气 |
| A. | A | B. | B | C. | C | D. | D |

 ;锂暴露在湿空气中时,会迅速地失去金属光泽、表面开始变黑,更长时间则变成白色.生成的化合物是氮化锂、氢氧化锂,最终生成碳酸锂.写出生成氮化锂的化学方程式6Li+N2=2Li3N.锂在空气中燃烧,发出浅蓝色的火焰,放出浓厚的白烟,生成相应氧化物Li2O(填化学式).
;锂暴露在湿空气中时,会迅速地失去金属光泽、表面开始变黑,更长时间则变成白色.生成的化合物是氮化锂、氢氧化锂,最终生成碳酸锂.写出生成氮化锂的化学方程式6Li+N2=2Li3N.锂在空气中燃烧,发出浅蓝色的火焰,放出浓厚的白烟,生成相应氧化物Li2O(填化学式).