题目内容
海水是巨大的资源宝库,可以进行综合利用。从海水中提取食盐和溴的过程如下:

(1)请写出一种海水淡化的方法:______________。
(2)步骤Ⅰ获得Br2的离子方程式为_________________________________________;
(3)步骤Ⅱ用SO2水溶液吸收Br2,使溴蒸气转化为氢溴酸以达到富集的目的。其反应的化学方程式为Br2+SO2+2H2O=H2SO4+2HBr,在该反应中,氧化剂是__________(填化学式)。若反应中生成2molHBr,则消耗________molSO2,若完全吸收后的酸溶液体积为500mL,则溶液中氢离子浓度为________mol/L。
(4)根据上述反应判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是________________。
(1)蒸馏法(其他合理答案均可);(2)Cl2+2Br-=Br2+2Cl-;(3)Br2;1;8;
(4)Cl2>Br2>SO2

练习册系列答案
相关题目
海水是巨大的资源宝库,下列关于海水综合利用的说法错误的是( )
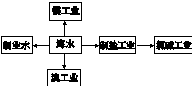

| A、海水制淡水主要有蒸馏法、电渗析法、离子交换法等 | B、海水制盐、发展氯碱工业都是发生物理变化 | C、海水提溴过程中先通入Cl2将溴离子氧化为溴单质 | D、工业上用电解熔融MgCl2的方法制取金属镁 |




