题目内容
在下列反应中,既属于离子反应又属于氧化还原反应的是( )
| A、BaCl2溶液和K2SO4溶液反应 |
| B、点燃H2和O2的混合气体 |
| C、NaOH溶液和CuSO4溶液反应 |
| D、Zn放入盐酸中 |
考点:离子反应发生的条件,氧化还原反应
专题:物质的性质和变化专题
分析:含元素化合价变化的反应为氧化还原反应,有离子参加的反应为离子反应,以此来解答.
解答:
解:A.属于离子反应,但没有元素的化合价变化,不属于氧化还原反应,故A不选;
B.属于氧化还原反应,但没有离子参加,不属于离子反应,故B不选;
C.属于离子反应,但没有元素的化合价变化,不属于氧化还原反应,故C不选;
D.HCl电离出离子,有离子参加,属于离子反应,且Zn、H元素的化合价变化,属于氧化还原反应,故D选;
故选D.
B.属于氧化还原反应,但没有离子参加,不属于离子反应,故B不选;
C.属于离子反应,但没有元素的化合价变化,不属于氧化还原反应,故C不选;
D.HCl电离出离子,有离子参加,属于离子反应,且Zn、H元素的化合价变化,属于氧化还原反应,故D选;
故选D.
点评:本题考查氧化还原反应和离子反应,为高频考点,把握溶液中的离子反应及反应中元素的化合价变化为解答的关键,侧重反应类型的考查,题目难度不大.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
有甲、乙、丙、丁四个集气瓶中分别盛有H2、Cl2、HCl、HBr中任意一种气体.若将甲和丙两气体混合,见光爆炸.若将丙、丁两气体混合后,瓶壁上出现深红棕色的液滴.则乙气体是( )
| A、H2 |
| B、Cl2 |
| C、HCl |
| D、HBr |
下列可以用来区分甲烷、乙烯、乙炔的是( )
| A、用溴水区分 |
| B、用酸性高锰酸钾溶液区分 |
| C、根据燃烧现象不同区分 |
| D、根据气味不同区分 |
下列说法中错误的是( )
| A、硅酸是不挥发性酸,因此不能由盐酸制得 |
| B、氢氟酸能和玻璃发生化学反应,所以氢氟酸要存放在塑料瓶中 |
| C、水玻璃有黏性,所以要存放在带橡胶塞的试剂瓶中 |
| D、烧碱溶液会腐蚀玻璃并生成硅酸钠,所以烧碱溶液要存放在带橡胶塞的试剂瓶里 |
下列离子组能大量共存的是( )
| A、Na+ Al3+ AlO2- Cl- |
| B、Mg2+ Al3+ SO42- NO3- |
| C、Ba2+ K+ SO42- NO3- |
| D、Na+ K+ ClO- S2- |
汽车尾气的无害化处理已成为当今汽车工业的一项重要课题,其基本原理是实现2NO(g)+2CO(g)?N2(g)+2CO2(g)的反应.关于该反应,下列说法正确的是( )
| A、只要使用合理的催化剂及载体,就可完全清除NO和CO |
| B、该反应达到平衡时v(NO)正=v(CO)逆 |
| C、假设该反应在密闭容器中进行,一段时间后达到平衡时c(NO)=c(CO) |
| D、使用性能好的催化剂可使反应的平衡常数增大 |
铜-锌原电池如图所示,下列叙述正确的是( )
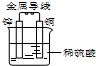

| A、氢离子在负极得电子 |
| B、锌为负极,发生氧化反应 |
| C、铜片上无气泡产生 |
| D、电子从铜片经金属导线流向锌片 |