题目内容
6. 如图小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片.观察:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面.以下有关解释合理的是( )
如图小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片.观察:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面.以下有关解释合理的是( )| A. | 生铁片中的碳是原电池的阳极,发生还原反应 | |
| B. | 墨水回升时,生铁片发生吸氧腐蚀 | |
| C. | 雨水酸性较强,生铁片仅发生析氢腐蚀 | |
| D. | 具支试管中溶液pH逐渐减小 |
分析 正常雨水的pH是5.6,溶液呈酸性,生铁中含有碳和铁,酸性条件下,生铁发生析氢腐蚀生成氢气,导致具支试管内气体压强大于大气压,导管内液面下降,当溶液呈弱酸性或中性时,生铁发生吸氧腐蚀,导致具支试管中气体压强小于大气压,导管内液面回升,略高于小试管液面,据此分析解答.
解答 解:正常雨水的pH是5.6,溶液呈酸性,生铁中含有碳和铁,酸性条件下,生铁发生析氢腐蚀生成氢气,导致具支试管内气体压强大于大气压,导管内液面下降,当溶液呈弱酸性或中性时,生铁发生吸氧腐蚀,导致具支试管中气体压强小于大气压,导管内液面回升,略高于小试管液面;
A.铁、碳和电解质溶液构成原电池,碳作正极,正极上得电子发生还原反应,故A错误;
B.墨水回升时,生铁片发生吸氧腐蚀,碳极上氧气得电子生成氢氧根离子,电极反应式为:O2+2H2O+4e-═4OH-,故B正确;
C.通过以上分析知,生铁片发生析氢腐蚀和吸氧腐蚀,故C错误;
D.具支试管中溶液,先呈酸性,发生析氢腐蚀时,溶液酸性逐渐减弱pH增大,当发生吸氧腐蚀时,负极上铁失电子生成亚铁离子,正极上生成氢氧根离子,亚铁离子和氢氧根离子生成氢氧化铁沉淀,溶液的pH不变,所以反应过程中,溶液的pH先增大达到一定值后不变,故D错误;
故选B.
点评 本题考查了金属的析氢腐蚀和吸氧腐蚀,明确雨水的酸碱性及生铁发生析氢腐蚀和吸氧腐蚀的条件是解本题的关键,难度不大,注意正常雨水的pH不是7而是5.6,为易错点.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
14.某冶炼厂以碳棒作电极,电解熔融状态的Al2O3,生成的氧气同时还与阳极碳棒反应生成CO和CO2,当生成54kg铝时,阳极消耗24kg碳,则阳极生成的CO和CO2中,CO和CO2的分子个数比为( )
| A. | 1﹕3 | B. | 1﹕2 | C. | 1﹕1 | D. | 2﹕1 |
18.在下列反应中,水作氧化剂的是( )
| A. | 2K+2H2O═2KOH+H2↑ | B. | Cl2+H2O═HCl+HClO | ||
| C. | 2F2+2H2O═4HF+O2 | D. | 2H2O2═2H2O+O2↑ |
15.氧化还原反应的实质和相应的规律是( )
| A. | 化合价的升降,化合价的升高和降低的总数相等 | |
| B. | 电子的转移,得电子总数和失电子总数相等 | |
| C. | 得氧和失氧,氧原子数目不变 | |
| D. | 物质的种类发生改变,质量守恒定律 |
16.在无色溶液中,下列离子能大量共存的是( )
| A. | NH4+、Na+、S2-、ClO- | B. | K +、SO42-、OH-、AlO2- | ||
| C. | K +、Fe3+、Cl-、NO3- | D. | Ba2+、Na+、OH-、CO32- |
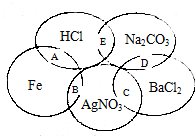 如图图为一五元环图案,小明在图案上依次写了五种物质,图中相交的两种物质均可发生化学反应,A、B、C、D、E表示其相应的化学反应.请回答下列问题:
如图图为一五元环图案,小明在图案上依次写了五种物质,图中相交的两种物质均可发生化学反应,A、B、C、D、E表示其相应的化学反应.请回答下列问题:


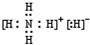 .
.