题目内容
已知铝与O2、O3在一定条件下均能反应,且都生成Al2O3.反应的热化学方程式如下:
4Al(s)+3O2(g)═2Al2O3(s);△H=-Q1 kJ/mol
4Al(s)+2O3(g)═2Al2O3(s);△H=-Q2 kJ/mol.Q1、Q2均大于0,且Q1<Q2,下列说法正确的组合是( )
①上述两个反应均为吸热反应;
②4mol固态Al和3mol气态O2所具有的总能量大于2mol固态Al2O3所具有的能量;
③等质量的O2、O3,O2的能量高; ④等物质的量的O2、O3,O3的能量高;
⑤由O2生成O3的反应为放热反应; ⑥由O2生成O3的反应为吸热反应.
4Al(s)+3O2(g)═2Al2O3(s);△H=-Q1 kJ/mol
4Al(s)+2O3(g)═2Al2O3(s);△H=-Q2 kJ/mol.Q1、Q2均大于0,且Q1<Q2,下列说法正确的组合是( )
①上述两个反应均为吸热反应;
②4mol固态Al和3mol气态O2所具有的总能量大于2mol固态Al2O3所具有的能量;
③等质量的O2、O3,O2的能量高; ④等物质的量的O2、O3,O3的能量高;
⑤由O2生成O3的反应为放热反应; ⑥由O2生成O3的反应为吸热反应.
| A、①②④ | B、②④⑥ |
| C、②③⑤ | D、③④⑥ |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:①焓变为负值,反应为放热反应;
②依据反应4Al(s)+3O2(g)═2Al2O3(s);△H=-Q1 kJ/mol是放热反应,结合反应前后能量守恒分析判断;
③依据热化学方程式计算氧气和臭氧转化的热化学方程式,判断能量变化;
④依据热化学方程式计算氧气和臭氧转化的热化学方程式,判断能量变化;
⑤依据热化学方程式计算氧气和臭氧转化的热化学方程式,判断能量变化;
⑥依据热化学方程式计算氧气和臭氧转化的热化学方程式,判断能量变化.
②依据反应4Al(s)+3O2(g)═2Al2O3(s);△H=-Q1 kJ/mol是放热反应,结合反应前后能量守恒分析判断;
③依据热化学方程式计算氧气和臭氧转化的热化学方程式,判断能量变化;
④依据热化学方程式计算氧气和臭氧转化的热化学方程式,判断能量变化;
⑤依据热化学方程式计算氧气和臭氧转化的热化学方程式,判断能量变化;
⑥依据热化学方程式计算氧气和臭氧转化的热化学方程式,判断能量变化.
解答:
解:已知铝与O2、O3在一定条件下均能反应,且都生成Al2O3.反应的热化学方程式如下:
①4Al(s)+3O2(g)═2Al2O3(s);△H=-Q1 kJ/mol
②4Al(s)+2O3(g)═2Al2O3(s);△H=-Q2 kJ/mol.Q1、Q2均大于0,且Q1<Q2,
①-②得到3O2(g)═2O3(g),△H=-Q1 kJ/mol+Q2 kJ/mol=-(Q1-Q2)kJ/mol,Q1<Q2,则△H>0;
①上述两个反应均为放热反应,故①错误;
②4Al(s)+3O2(g)═2Al2O3(s);△H=-Q1 kJ/mol,反应是放热反应,4mol固态Al和3mol气态O2所具有的总能量大于2mol固态Al2O3所具有的能量,故②正确;
③依据上述计算分析,等质量的O2、O3,O3的能量高,故③错误;
④等物质的量的O2、O3,O3的能量高,故④正确;
⑤由O2生成O3的反应为吸热反应,故⑤错误;
⑥由O2生成O3的反应为吸热反应,故⑥正确;
由上述分析可知②④⑥正确,
故选B.
①4Al(s)+3O2(g)═2Al2O3(s);△H=-Q1 kJ/mol
②4Al(s)+2O3(g)═2Al2O3(s);△H=-Q2 kJ/mol.Q1、Q2均大于0,且Q1<Q2,
①-②得到3O2(g)═2O3(g),△H=-Q1 kJ/mol+Q2 kJ/mol=-(Q1-Q2)kJ/mol,Q1<Q2,则△H>0;
①上述两个反应均为放热反应,故①错误;
②4Al(s)+3O2(g)═2Al2O3(s);△H=-Q1 kJ/mol,反应是放热反应,4mol固态Al和3mol气态O2所具有的总能量大于2mol固态Al2O3所具有的能量,故②正确;
③依据上述计算分析,等质量的O2、O3,O3的能量高,故③错误;
④等物质的量的O2、O3,O3的能量高,故④正确;
⑤由O2生成O3的反应为吸热反应,故⑤错误;
⑥由O2生成O3的反应为吸热反应,故⑥正确;
由上述分析可知②④⑥正确,
故选B.
点评:本题考查了化学反应能量变化分析,盖斯定律的计算应用,注意物质能量越高越活泼,掌握基础是关键,题目难度中等.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
已知在一定条件下2A(g)+B(g)?3C(g)△H=+Q kJ?mol-1.向一个容积不变的密闭容器甲中加入2mol A和1mol B,达平衡时A的转化率为90%,吸收的热量为Q1kJ;向另一个密闭容器乙中加入一定量C,达到平衡时C的浓度与甲相同,放出的热量为Q2 kJ,则下说法中正确的是( )
| A、起始时C的物质的量及C的转化率一定为3 mol和10% |
| B、Q1>Q2 |
| C、Q2一定小于Q1 |
| D、若乙容器是一个体积不变的绝热容器,则反应达平衡后,乙中的压强一定大于甲 |
化学反应都伴随有能量变化.下列反应中不能由化学能转化为电能的是( )
| A、酸碱中和反应 |
| B、金属锌与硫酸铜溶液反应 |
| C、乙醇燃烧 |
| D、金属铜溶于氯化铁溶液 |
已知二氯苯有3种同分异构体,则四氯苯的同分异构体有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
下列说法正确的是( )
A、 与足量的H2加成产物的名称为2,2-二甲基-5-乙基已烷 与足量的H2加成产物的名称为2,2-二甲基-5-乙基已烷 |
| B、乙酸、硬脂酸、油酸属于同系物 |
C、莽草酸 可以发生氧化、还原、加聚、缩聚等反应 可以发生氧化、还原、加聚、缩聚等反应 |
D、1mol化合物 分别与足量的浓溴水、足量的NaOH溶液反应,消耗Br2和NaOH的物质的量相等 分别与足量的浓溴水、足量的NaOH溶液反应,消耗Br2和NaOH的物质的量相等 |
反应H2(g)+Br2(l)═2HBr(g)在25℃、101kPa下进行,已知生成2molHBr放出热量为72kJ,蒸发1mol Br2(l)需要吸收的能量为30kJ,其他相关数据如下表:则表中a为( )
| 1mol分子中的化学键断时需要吸收能量/kJ | H2(g) | Br2(g) | HBr(g) |
| 436 | a | 369 |
| A、404 | B、260 |
| C、230 | D、200 |
聚四氟乙烯(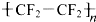 )是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
)是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
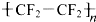 )是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
)是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )| A、属于高分子化合物 |
| B、单体是CF2=CF2 |
| C、可由加聚反应得到 |
| D、能使高锰酸钾酸性溶液褪色 |
某有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,由此可以得出该有机物( )
| A、分子中C、H、O的个数比为1:2:3 |
| B、分子中C和H的个数比为1:2 |
| C、分子中肯定不一定含氧原子 |
| D、分子中肯定含有氧原子 |