题目内容
有关物质的转化关系如下图所示(部分物质和条件已略去).B、C、E是常见气体;A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;G的焰色反应显黄色;I的溶液呈黄色.

请回答下列问题:
(1)F的化学式为 .
(2)E的电子式为 .
(3)写出C与D溶液反应的化学方程式: .
(4)写出Y和D溶液反应的离子方程式: .

请回答下列问题:
(1)F的化学式为
(2)E的电子式为
(3)写出C与D溶液反应的化学方程式:
(4)写出Y和D溶液反应的离子方程式:
考点:无机物的推断
专题:
分析:金属Y既能与强酸反应,又能与强碱反应,则Y为Al;G的焰色反应显黄色,含有Na元素,结合转化关系,由元素守恒可知金属A为Na,与水反应生成D与气体B,则B为H2、D为NaOH,I的溶液呈黄色,结合转化关系可知,含有Fe3+,则金属X为Fe,气体C具有强氧化性,可推知C为Cl2,则E为HCl、H为FeCl2,I为FeCl3,C与Y反应生成F为AlCl3,由于F与D反应生成G,且D与Y反应也得到G,故G为NaAlO2,以此来解答.
解答:
解:金属Y既能与强酸反应,又能与强碱反应,则Y为Al;G的焰色反应显黄色,含有Na元素,结合转化关系,由元素守恒可知金属A为Na,与水反应生成D与气体B,则B为H2、D为NaOH,I的溶液呈黄色,结合转化关系可知,含有Fe3+,则金属X为Fe,气体C具有强氧化性,可推知C为Cl2,则E为HCl、H为FeCl2,I为FeCl3,C与Y反应生成F为AlCl3,由于F与D反应生成G,且D与Y反应也得到G,故G为NaAlO2,
(1)由上述分析可知,F的化学式为AlCl3,故答案为:AlCl3;
(2)E为HCl,其电子式为 ,故答案为:
,故答案为: ;
;
(3)C与D溶液反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O,故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
(4)Y和D溶液反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(1)由上述分析可知,F的化学式为AlCl3,故答案为:AlCl3;
(2)E为HCl,其电子式为
 ,故答案为:
,故答案为: ;
;(3)C与D溶液反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O,故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
(4)Y和D溶液反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评:本题考查无机物推断,为高频考点,涉及Fe、Al、Cl元素单质化合物知识,把握Y的性质及G的焰色反应、I的溶液呈黄色等是推断突破口,侧重分析与推断能力的综合考查,题目难度中等.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
X、Y、Z、W、Q是五种短周期元素,它们在周期表中的位置如图.下列说法不正确的是( )
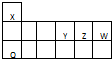

| A、Z与W可形成的化合物在5种以上 |
| B、Z、W、Q三种元素形成的化合物,其水溶液一定呈中性 |
| C、X、Y、Z、W形成的化合物的化学式可以是Y2X7W2Z |
| D、X与Y、Z、W均可形成原子个数比为2:1的化合物 |
电化学降解NO3-的原理如图所示.下列说法正确的是( )
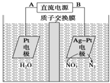

| A、电源正极为B |
| B、阳极反应式为2NO3-+6H2O+10e-=N2↑+12OH- |
| C、当产生N211.2L时,电路中通过的电子数为5NA |
| D、若电解过程中转移了2 mol电子,则两极产生的气体的质量差为10.4g |
当可逆反应2SO2(g)+O2(g)═2SO3(g)达到平衡后,向平衡体系中充入一定量的18O2气体,当反应再次达到平衡时,18O原子( )
| A、只存在于O2中 |
| B、只存于SO3中 |
| C、同时存在于O2和SO3中 |
| D、同时存在于O2、SO2和SO3中 |
提纯下列物质(括号内物质为杂质)选用的试剂和分离方法都正确的是( )
| 物 质 | 除杂试剂 | 分离方法 | |
| A | I2(CCl4) | -- | 过滤 |
| B | Cl2(HCl) | NaOH溶液 | 洗气 |
| C | KNO3(KCl) | -- | 降温结晶 |
| D | Al(Fe) | NaOH溶液 | 过滤 |
| A、A | B、B | C、C | D、D |
下列有关物质的性质或应用正确的是( )
| A、氧化铝常用于制造耐火材料 |
| B、浓硫酸用于干燥氨气 |
| C、生产水泥的主要原料是黏土、纯碱 |
| D、Na2O用作呼吸面具的供氧剂 |
通过一步反应能实现下列转化的是( )
| A、Si→SiO2→H2SiO3→Na2SiO3 |
| B、S→SO3→H2SO4→Na2SO4 |
| C、Na→NaOH→Na2CO3→NaCl |
| D、Al→AlCl3→Al(OH)3→NaAlO2 |
对有机物 的化学性质叙述错误的是( )
的化学性质叙述错误的是( )
 的化学性质叙述错误的是( )
的化学性质叙述错误的是( )| A、加热时能被新制的银氨溶液氧化 |
| B、能使酸性KMnO4溶液褪色 |
| C、能发生加聚反应 |
| D、1 mol该物质只能与l molH2加成 |
金属活动顺序表中氢前金属与酸溶液中的H+反应可生成H2.以下方法不能加快Fe与稀硫酸反应制取H2的速率的是( )
| A、用98%的浓硫酸代替稀硫酸制取H2 |
| B、适当加热反应体系 |
| C、用粉末状的铁代替块状或片状的铁 |
| D、加入几滴硫酸铜溶液 |