题目内容
在25℃时,分别用pH=9、pH=10的两种氨水中和同浓度、同体积的盐酸,消耗氨水的体积分别为V1和V2,则V1和V2的关系是( )
分析:同一弱电解质溶液中,溶液的浓度越大,其电离程度越大,中和等浓度等体积的盐酸所用的氨水体积与氨水的浓度有关.
解答:解:pH=9的氨水中c(OH-)=10-5 mol/L,pH=10的溶液中c(OH-)=10-4 mol/L,根据题意知,C1(NH3.H2O)V1=C2(NH3.H2O)V2,弱电解质溶液中,溶液浓度越大弱电解质电离程度越小,所以
=
>10,
所以得V1>10V2,故选B.
| V1 |
| V2 |
| c2 |
| c1 |
所以得V1>10V2,故选B.
点评:本题考查了弱电解质的电离,明确弱电解质的电离程度与溶液浓度的关系是解本题关键,难度中等.

练习册系列答案
相关题目
 (2013?淄博二模)(1)在固定容积为2L的密闭容器中通入NO和CO各2mol发生反应:
(2013?淄博二模)(1)在固定容积为2L的密闭容器中通入NO和CO各2mol发生反应:

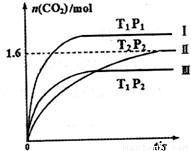
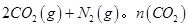 随温度(T)、压强(P)和时间(t)的变化曲线如图所示。请回答下列问题:
随温度(T)、压强(P)和时间(t)的变化曲线如图所示。请回答下列问题: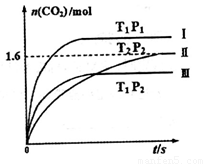
 、
、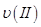 、
、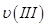 ,则三者大小关系为______________。
,则三者大小关系为______________。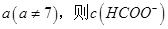 ________
________ (填“>”、“=”或“<”),则HCOO-的水解平衡常数(Kh)可近似表示为______________(用含a的代数式表示)。
(填“>”、“=”或“<”),则HCOO-的水解平衡常数(Kh)可近似表示为______________(用含a的代数式表示)。 b.
b.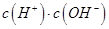 c.
c.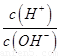 d.
d.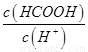
 2CO2(g)+N2(g).n(CO2)随温度(T)、压强(P)和时间(t)的变化曲线如图所示.请回答下列问题:
2CO2(g)+N2(g).n(CO2)随温度(T)、压强(P)和时间(t)的变化曲线如图所示.请回答下列问题: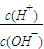 d.
d. .
.