题目内容
关于下列图示的说法中正确的是( )


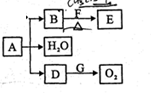
| A、图①装置用于分离沸点相差较大的互溶液体混合物 |
| B、图②装置用于研究不同催化剂对反应速率的影响 |
| C、图③中电流计的指针不发生偏转 |
| D、对反应:A(s)+2B(g)?xC(g);根据图④可以求出x=2 |
考点:化学实验方案的评价
专题:
分析:A.蒸馏时温度计测定馏分温度;
B.研究不同催化剂对反应速率影响时,过氧化氢浓度应该相等;
C.该装置构成原电池,有电流产生;
D.根据图片知,2min时,C参加反应的物质的量=(0.2-0)mol=0.2mol,B反应的物质的量=(0.3-0.1)=0.2mol,相同时间内各物质的反应物质的量之比等于其计量数之比,所以B、C的计量数相等.
B.研究不同催化剂对反应速率影响时,过氧化氢浓度应该相等;
C.该装置构成原电池,有电流产生;
D.根据图片知,2min时,C参加反应的物质的量=(0.2-0)mol=0.2mol,B反应的物质的量=(0.3-0.1)=0.2mol,相同时间内各物质的反应物质的量之比等于其计量数之比,所以B、C的计量数相等.
解答:
解:A.蒸馏时温度计测定馏分温度,所以温度计水银球应该位于蒸馏烧瓶支管口处,故A错误;
B.研究不同催化剂对反应速率影响时,过氧化氢浓度应该相等,否则无法比较,故B错误;
C.该装置构成原电池,有电流产生,通入氧气的电极是正极,Cu作负极,负极上Cu失电子生成铜离子,故C错误;
D.根据图片知,2min时,C参加反应的物质的量=(0.2-0)mol=0.2mol,B反应的物质的量=(0.3-0.1)=0.2mol,相同时间内各物质的反应物质的量之比等于其计量数之比,所以B、C的计量数相等,对反应:A(s)+2B(g)?xC(g),根据图④可以求出x=2,故D正确;
故选D.
B.研究不同催化剂对反应速率影响时,过氧化氢浓度应该相等,否则无法比较,故B错误;
C.该装置构成原电池,有电流产生,通入氧气的电极是正极,Cu作负极,负极上Cu失电子生成铜离子,故C错误;
D.根据图片知,2min时,C参加反应的物质的量=(0.2-0)mol=0.2mol,B反应的物质的量=(0.3-0.1)=0.2mol,相同时间内各物质的反应物质的量之比等于其计量数之比,所以B、C的计量数相等,对反应:A(s)+2B(g)?xC(g),根据图④可以求出x=2,故D正确;
故选D.
点评:本题考查化学实验方案评价,为高考高频点,涉及物质分离和提纯、原电池原理、化学反应速率影响因素等知识点,明确实验原理是解本题关键,把握物质性质、基本操作规范性即可解答,易错选项是C.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
下列溶液中,微粒浓度关系正确的是( )
| A、常温下,pH=6的醋酸与醋酸钠组成的混合溶液中:c(Na+)>c(CH3COO-) |
| B、将Cl2通入过量KOH溶液中:c(ClO-)+c(Cl-)=c(K+) |
| C、向硝酸钙溶液加稀盐酸得到pH=4的溶液中:2c(Ca2+)=c(NO3-) |
| D、0.1mol?L-1的醋酸的pH=a,0.01mol?L-1的醋酸的pH=b,则a+1=b |
下列有关说法错误的是( )
A、 既可以表示10B的原子结构,也可以表示11B的原子结构 既可以表示10B的原子结构,也可以表示11B的原子结构 |
| B、H++OH-=H2O既可以表示NaOH与盐酸反应,也可以表示Ba(OH)2与硫酸反应 |
| C、CH4分子的空间结构与NH4+的相同 |
| D、C2H4O2既可以表示乙酸的分子式,也可以表示甲酸甲酯的分子式 |
 国庆节期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,下列关于该物质的说法正确的是( )
国庆节期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,下列关于该物质的说法正确的是( )| A、其分子式为C15H21O4 |
| B、该有机物能发生取代、加成和水解反应 |
| C、1mol的该有机物与足量的钠反应产生1molH2 |
| D、该有机物不能使酸性KMnO4溶液褪色 |
下列各组离子在溶液中能大量共存的是( )
| A、Na+、OH-、S2O32-、Cl- |
| B、Fe2+、K+、[Fe(CN)6]3-、NO3- |
| C、H+、C2O42-、MnO4-、SO42- |
| D、Na+、Ca2+、AlO2-、HCO3- |



 (Ⅰ)已知X、Y、Z、W为短周期四种常见元素,其中X是原子半径最小的元素,Y原子的外层电子数是内层电子数二倍,Z能和X形成两种常见的液态化合物,W元素的单质既能与盐酸反应能与NaOH溶液反应,试回答下列问题:
(Ⅰ)已知X、Y、Z、W为短周期四种常见元素,其中X是原子半径最小的元素,Y原子的外层电子数是内层电子数二倍,Z能和X形成两种常见的液态化合物,W元素的单质既能与盐酸反应能与NaOH溶液反应,试回答下列问题:


