题目内容
2.下列事实可以说明 苯分子结构中不存在C-C单键和C=C双键交替结构的是 ①苯不能使溴水和酸性高锰酸钾溶液褪色 ②苯在一定条件下既能发生取代反应,又能发生加成反应 ③邻二甲苯只有一种结构 ④苯环上碳碳键的键长相等( )| A. | 全部 | B. | 只有①④ | C. | 只有①③④ | D. | 只有①②④ |
分析 ①依据苯的性质判断苯的结构,高锰酸钾溶液具有强氧化性,遇到含双键或三键等不饱和键的物质会褪色分析;
②依据与氢气发生加成反应是不饱和键的性质分析;
③根据同分异构体数目解答;
④单键键长与双键键长不相等;
解答 解:①苯不能使酸性高锰酸钾溶液褪色,说明苯分子中不含碳碳双键,可以证明苯环结构中不存在C-C单键与C=C双键的交替结构,故①正确;
②苯能在一定条件下跟H2加成生成环己烷,发生加成反应是双键或三键具有的性质,不能证明苯环结构中不存在C-C单键与C=C双键的交替结构,故②错误;
③如果是单双键交替结构,邻二甲苯的结构有两种,一种是两个甲基夹C-C,另一种是两个甲基夹C=C.邻二甲苯只有一种结构,说明苯环结构中的化学键只有一种,不存在C-C单键与C=C双键的交替结构,故③正确;
④苯环上碳碳键的键长相等,说明苯分子结构中不存在C-C单键和C=C双键交替结构,故④正确;
故选:C.
点评 本题考查苯的结构与性质,难度不大,综合性较大,要求知识掌握全面,能运用知识分析和解决问题,侧重学生分析解决问题的能力的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.关于钠及其化合物的说法正确的是( )
| A. | 将钠块投入到硫酸铜溶液中,可析出单质铜 | |
| B. | 将钠块长时间暴露在空气中的最终产物是Na2CO3 | |
| C. | Na2O与Na2O2阴阳离子个数比相同 | |
| D. | Na2O2能使品红溶液褪色且原理与SO2相同 |
10.把等物质的量的CuSO4、FeCl3和锌粉置于足量的水中,充分反应,反应后的溶液中大量存在的金属阳离子是( )
| A. | Cu2+、Fe3+、Fe2+、Zn2+ | B. | Fe3+、Fe2+、Zn2+ | ||
| C. | Cu2+、Fe3+、Zn2+ | D. | Cu2+、Fe2+、Zn2+ |
17.反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在2L的密闭容器中进行,1分钟后,NH3减少了0.12mol,则平均每秒钟浓度变化正确的是( )
| A. | NO:0.001mol•L-1 | B. | H2O:0.002mol•L-1 | ||
| C. | NH3:0.002mol•L-1 | D. | O2:0.0025mol•L-1 |
7.下列有关NA叙述正确的是( )
| A. | 标准状况下,1molSO3的气体体积为22.4L | |
| B. | 1mol铁粉与过量Cl2反应时,转移电子数为2NA | |
| C. | 含有2NA个氧原子的D2O质量为40g | |
| D. | 16gO2分子中含有的氧原子数为0.5NA |
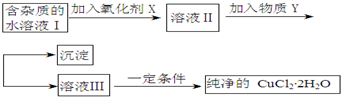
14.铁铜单质及其化合物的应用范围很广.现有含氯化亚铁杂质的氯化铜晶体(CuCl2•2H2O),为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按照如图步骤进行提纯:
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见表:
请回答下列问题:
(1)下列最适合作氧化剂X的是C
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)加入的物质Y是CuO[或Cu(OH)2、CuCO3、Cu2(OH)2CO3]如果不用物质Y而直接用可溶性碱溶液不能 (填“能”或者“不能”)达到目的.若不能,试解释原因加碱使Fe3+沉淀的同时也能使Cu2+沉淀(若填“能”,此空不用回答)
(3)最后不能(填“能”或者“不能”)直接蒸发得到CuCl2•2H2O?若不能,应该如何操作才能得到CuCl2•2H2O应在HCl气流中加热蒸发结晶(若填“能”,此空不用回答)
(4)若向溶液Ⅱ中加入碳酸钙,产生的现象是碳酸钙溶解,产生气泡和红褐色沉淀
(5)若向溶液Ⅱ中加入镁粉,产生的气体是氢气,试解释原因镁粉与氯化铁、氯化铜水解生成的氢离子反应生成氢气.

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
(1)下列最适合作氧化剂X的是C
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)加入的物质Y是CuO[或Cu(OH)2、CuCO3、Cu2(OH)2CO3]如果不用物质Y而直接用可溶性碱溶液不能 (填“能”或者“不能”)达到目的.若不能,试解释原因加碱使Fe3+沉淀的同时也能使Cu2+沉淀(若填“能”,此空不用回答)
(3)最后不能(填“能”或者“不能”)直接蒸发得到CuCl2•2H2O?若不能,应该如何操作才能得到CuCl2•2H2O应在HCl气流中加热蒸发结晶(若填“能”,此空不用回答)
(4)若向溶液Ⅱ中加入碳酸钙,产生的现象是碳酸钙溶解,产生气泡和红褐色沉淀
(5)若向溶液Ⅱ中加入镁粉,产生的气体是氢气,试解释原因镁粉与氯化铁、氯化铜水解生成的氢离子反应生成氢气.
11.碱性锌锰电池是一种常见的一次电池,应用非常广泛,其工作时发生如下反应:Zn+2MnO2+H2O=2MnOOH+Zn(OH)2,下列说法正确的是( )
| A. | Zn为负极,MnO2为正极 | |
| B. | Zn为正极,MnO2为负极 | |
| C. | 工作时电子由MnO2经外电路流向Zn极 | |
| D. | Zn电极发生还原反应,MnO2电极发生氧化反应 |