题目内容
已知 N2+3H2?2NH3△H<0,若将此反应设计成燃料电池,盐酸为电解质溶液,下列说法错误的是( )
| A、燃料电池正极充入N2 |
| B、电池的负极反应为H2-2e-=2H+ |
| C、电池的正极反应为 N2+6e-+6H+═2NH3 |
| D、电池工作时正极发生还原反应 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:N2、H2为电极反应物,以HCl为电解质溶液制成新型燃料电池,正极发生还原反应,N2得电子生成NH4+,负极发生氧化反应:H2-2e-=2H+,以此分析解题.
解答:
解:A、燃料电池正极发生还原反应,充入N2,故A正确;
B、电池的负极反应为H2-2e-=2H+,故B正确;
C、电池的正极反应为 N2+6e-+8H+═2NH4+,故C错误;
D、电池工作时正极发生还原反应,故D正确;
故选C.
B、电池的负极反应为H2-2e-=2H+,故B正确;
C、电池的正极反应为 N2+6e-+8H+═2NH4+,故C错误;
D、电池工作时正极发生还原反应,故D正确;
故选C.
点评:本题考查原电池的原理,以及电极反应方程式的书写,比较容易.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
烷烃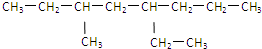 是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )
是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )
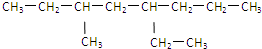 是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )
是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )| A、1种 | B、2种 | C、3种 | D、4种 |
下列化合物分子中既有离子键又有共价键的是( )
| A、BaCl2 |
| B、Na2O |
| C、(NH4)2SO4 |
| D、H2SO4 |
往下列溶液中,通入足量CO2气体,最终能析出固体的是( )
| A、澄清石灰水 |
| B、饱和Na2CO3溶液 |
| C、CaCl2溶液 |
| D、盐酸 |
有t℃的a g KCl不饱和溶液,其质量分数为w1,采取措施后使其变为b g饱和溶液,其溶质质量分数为w2,下列说法正确的是( )
| A、a一定小于或等于b |
| B、aw1一定等于b w2 |
| C、t℃时KCl溶解度一定大于100w1 |
| D、w1一定大于w2 |
下列反应的能量变化属于吸热反应的是( )
| A、氯化铵与Ba(OH)2?8H2O的反应 |
| B、氢氧化钠溶液与盐酸反应 |
| C、锌片与稀硫酸反应 |
| D、钠与冷水反应 |
 某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验
某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验