题目内容
某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结,归纳正确的是
①常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有
c (Na+) + c(H+)=c(OH-) + c(CH3COO-)
②对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,生成物的百分含量一定增加
③常温下,AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同
④常温下,已知醋酸电离平衡常数为Ka,醋酸根水解平衡常数为Kh,水的离子积为Kw,则有:Ka ∶Kh=Kw
A.①④ B.①②④ C.②③ D.③④
A
【解析】
试题分析:①常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,根据电荷守恒则有c (Na+) + c(H+)=c(OH-) + c(CH3COO-),正确;②对已建立化学平衡的某可逆反应,若将生成物从平衡体系中分离出来使化学平衡向正反应方向移动时,生成物的百分含量一般会减小,错误;③常温下,同物质的量浓度的CaCl2和NaCl溶液中氯离子浓度前者是后者的2倍,故AgCl在CaCl2溶液中的溶解度小,错误;④常温下,醋酸电离平衡常数为Ka=[CH3COO-]·[H+]/[CH3COOH],醋酸根水解平衡常数Kh=[CH3COOH]·[OH-]/ [CH3COO-],水的离子积为Kw=[H+]·[OH-],则有:Ka ∶Kh=Kw,正确,选A。
考点:考查电解质溶液中的离子平衡。

练习册系列答案
相关题目
元素X~Z是元素周期表中4种主族元素,其性质或结构信息如下表,有关下列元素的描述错误的是( )
| 元素 | X | Y | W | Z |
| 相关信息 | 用硫酸处理海藻灰时,可得通常状况下为紫黑色的固体,其制剂可用来消毒. | 工业上在冰晶石存在的条件下,用电解法制取其单质. | 最早是在用氯气处理提取食盐后的盐水母液中发现的,被称作“海洋元素”. | 原子的电子总数是最外层电子数的6倍 |
| A、实验室可在海藻灰的浸出液中滴加双氧水来制取元素X的单质 |
| B、元素X、Y的单质充分混合后滴加少量水,可看到大量紫色蒸汽生成,说明该反应会放出大量的热 |
| C、元素X的气态氢化物的沸点高于元素W的气态氢化物的沸点 |
| D、元素Z是一种较活泼的金属元素,可用铝热法从Z的氧化物中制备Z的单质 |


 SO42—+Cr3++H2O(未配平),则每消耗0.4mol Cr2O72—转移__________mol e-。
SO42—+Cr3++H2O(未配平),则每消耗0.4mol Cr2O72—转移__________mol e-。
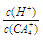 的值将 (填“增大”、“减少”或“不变”)。
的值将 (填“增大”、“减少”或“不变”)。