题目内容
2.如图为铜锌原电池示意图,下列说法错误的是( )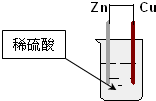
| A. | 铜片表面有气泡产生 | B. | 负极反应为:Cu-2e-=Cu2+ | ||
| C. | 锌为负极,铜为正极 | D. | 电子通过锌片经导线流向铜片 |
分析 锌铜原电池依据装置图分析,锌做负极失电子发生氧化反应生成锌离子,铜做正极,溶液中氢离子得到电子生成氢气,发生还原反应,电子流向从负极沿导线流向正极,溶液中阳离子移向正极,以此解答该题.
解答 解:A.铜作正极,正极上氢离子得电子发生还原反应生成氢气,所以Cu上有气泡生成,故A正确;
B.负极是锌失电子发生氧化反应,电极反应为Zn-2e-=Zn2+,故B错误;
C.锌比铜活泼,应为原电池的负极,铜为正极,故C正确;
D.电子由负极移向正极,电子由锌片通过导线流向铜,故D正确.
故选B.
点评 本题考查学生原电池的工作原理,为高频考点,侧重于双基的考查,注意把握正负极的判断及电子的流向,题目难度不大.

练习册系列答案
相关题目
17.用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).
下列说法中,正确的是( )
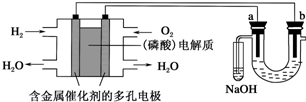
下列说法中,正确的是( )

| A. | 电池工作时,正极反应式为O2+2H2O+4e-═4OH- | |
| B. | 电解时,a电极周围首先放电的是Cl-,而不是Br- | |
| C. | 电解时,电子流动路径是:负极-→外电路-→阴极-→溶液-→阳极-→正极 | |
| D. | 忽略能量损耗,当电池中消耗0.02 g H2时,b极周围会产生0.02 g H2 |
7.下列实验操作中正确的是( )
| A. | 用胶头滴管向试管中加入液体时,为防止滴在试管外面,应将滴管尖嘴处伸入试管口中 | |
| B. | 硫酸必须用棕色试剂瓶保存 | |
| C. | 浓烧碱液沾到皮肤上应立即用大量水冲洗,然后涂上稀硼酸溶液 | |
| D. | 蒸馏时,应将温度计的水银球插入液面以下 |
14.某气体在标准状况下体积是4.48L,质量是14.2g,该气体的摩尔质量是( )
| A. | 71 | B. | 71 g•mol-1 | C. | 28.4 | D. | 28.4 g•mol-1 |
11. 往含有少量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生如图变化,四条曲线(c和d图象部分重叠)溶液中离子的对应关系,正确的是( )
往含有少量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生如图变化,四条曲线(c和d图象部分重叠)溶液中离子的对应关系,正确的是( )
 往含有少量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生如图变化,四条曲线(c和d图象部分重叠)溶液中离子的对应关系,正确的是( )
往含有少量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生如图变化,四条曲线(c和d图象部分重叠)溶液中离子的对应关系,正确的是( )| A. | a:Cl-b:K+ c:CO32- d:HCO3- | |
| B. | a:K+ b:CO32- c:Cl- d:HCO3- | |
| C. | a:K+ b:CO32- c:HCO3- d:Cl- | |
| D. | a:K+ b:HCO3- c:Cl- d:CO32- |

 用图示的装置进行电解,通电一段时间后,发现Pt电极上有气泡冒出.
用图示的装置进行电解,通电一段时间后,发现Pt电极上有气泡冒出.