题目内容
17.下列各组物质中,所含分子数相同的是( )| A. | 10gH2和10gO2 | B. | 11.2L(标准状况)H2O和0.5molBr2 | ||
| C. | 5.6LN2(标准状况)和11gCO2 | D. | 224mLH2(标准状况)和0.1molN2 |
分析 根据N=nNA可知,物质的量相同时含有分子数相同,根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$对各选项进行计算即可.
解答 解:A.氢气和氧气的摩尔质量不同,根据n=$\frac{m}{M}$可知10gH2和10gO2的物质的量不相等,含有分子数一定不相等,故A错误;
B.标准状况下水的状态不是气态,则水的物质的量不是0.5mol,二者物质的量不相等,则含有分子数不同,故B错误;
C.标准状况下5.6L氮气的物质的量为:$\frac{5.6L}{22.4L/mol}$=0.25mol,11g二氧化碳的物质的量为:$\frac{11g}{44g/mol}$=0.25mol,二者物质的量相等,则含有分子数相同,故C正确;
D.标准状况下224mLH2的物质的量为:$\frac{0.224L}{22.4L/mol}$=0.01mol,与0.1molN2的物质的量不相等,则二者含有的分子数不同,故D错误;
故选C.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与阿伏伽德罗常数、摩尔质量、气体摩尔体积之间的关系即可解答,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.将含有氧化铁的铁片投入足量稀硫酸中,直到铁片完全溶解,经分析该溶液中无Fe3+,且生成的Fe2+与生成的H2的物质的量之比为2:1,则原混合物中Fe2O3与铁的物质的量之比为( )
| A. | 1:1 | B. | 1:2 | C. | 1:4 | D. | 3:1 |
5.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1mol碳正离子(CH3+)所含质子总数为8NA | |
| B. | 常温常压下,46gNO2和N2O4混和气体中含原子总数为3NA | |
| C. | 标准状况下,11.2L氟化氢中含有氟原子的数目为0.5NA | |
| D. | 14g14C原子形成的石墨中,所含C-C健的个数为NA |
12.下列选项中不能说明硫元素的非金属性强于碳元素的是( )
| A. | 硫酸酸性强于碳酸 | |
| B. | 硫与氢气加热到500℃生成H2S,碳与氢气隔绝空气加热到1200℃生成CH4 | |
| C. | CS2中硫显示-2价 | |
| D. | 硫位于ⅥA族,碳位于ⅣA族 |
5.下列说法正确的是( )
| A. | 摩尔是联系宏观和微观的物理量 | |
| B. | Na的摩尔质量为23g/mol | |
| C. | 非标准状况下气体摩尔体积不可能为22.4 L | |
| D. | 1mol氢的质量为2g |
12.某研究小组为探究铁发生电化学腐蚀的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化(结果如图2).下列叙述错误的是( )


| A. | 图2中,t2时容器中压强明显小于起始压强是因为铁粉发生了吸氧腐蚀 | |
| B. | 碳粉表面的电极反应式只有:2H2O+O2+4e-═4OH- | |
| C. | 碳粉表面一定发生了还原反应 | |
| D. | 图3中,发生腐蚀时电子转移方向如箭头所示 |
9.下列说法正确的是( )
| A. | 弱电解质溶液中至少存在两种共价化合物分子 | |
| B. | 强电解质都是离子化合物,弱电解质都是共价化合物 | |
| C. | NH3属于非电解质,但其水溶液能够导电 | |
| D. | 同位素单质混合在一起一般是纯净物 |
10.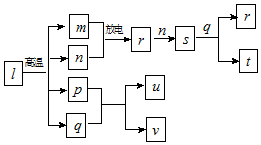 短周期主族元素X、Y、Z、W的原子序数依次增大.在图所示物质转化关系中,l是由该四种元素组成的离子化合物,m是Y的单质,n是Z的单质,p是W的单质,其余为由上述的两种或三种元素组成的化合物.u的水溶液具有漂白性;常温时,0.01mol•L-1t与0.01mol•L-1v溶液的pH均为2.
短周期主族元素X、Y、Z、W的原子序数依次增大.在图所示物质转化关系中,l是由该四种元素组成的离子化合物,m是Y的单质,n是Z的单质,p是W的单质,其余为由上述的两种或三种元素组成的化合物.u的水溶液具有漂白性;常温时,0.01mol•L-1t与0.01mol•L-1v溶液的pH均为2.
下列说法正确的是( )
 短周期主族元素X、Y、Z、W的原子序数依次增大.在图所示物质转化关系中,l是由该四种元素组成的离子化合物,m是Y的单质,n是Z的单质,p是W的单质,其余为由上述的两种或三种元素组成的化合物.u的水溶液具有漂白性;常温时,0.01mol•L-1t与0.01mol•L-1v溶液的pH均为2.
短周期主族元素X、Y、Z、W的原子序数依次增大.在图所示物质转化关系中,l是由该四种元素组成的离子化合物,m是Y的单质,n是Z的单质,p是W的单质,其余为由上述的两种或三种元素组成的化合物.u的水溶液具有漂白性;常温时,0.01mol•L-1t与0.01mol•L-1v溶液的pH均为2.下列说法正确的是( )
| A. | 原子半径:r(X)<r(Z)<r(Y) | |
| B. | 简单氢化物的稳定性:Y>Z>W | |
| C. | W的氧化物的水化物的酸性一定比Y的强 | |
| D. | X、Y、Z三种元素形成的化合物只能抑制水的电离 |