题目内容
7.0.8molCO2和0.8molCO中含有碳原子的物质的量之比为1:1,含有氧元素的质量之比为2:1,两物质中含有电子的物质的量之比为11:7.分析 二者含有碳原子的物质的量之比等于二者物质的量之比;结合二者分子组成及m=nM计算出二者含有氧元素质量之比;二氧化碳、一氧化碳分子分别含有22、14个电子,结合二者物质的量计算出含有电子的物质的量之比.
解答 解:0.8molCO2和0.8molCO中含有碳原子的物质的量之比=(0.8mol×1):(0.8mol×1)=1:1;
二者含有氧元素的质量之比=(16g/mol×0.8mol×2):(16g/mol×0.8mol×1)=2:1;
二者含有电子的物质的量之比=(0.8mol×22):(0.8mol×14)=11:7,
故答案为:1:1;2:1;11:7.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与其它物理量之间的转化关系即可解答,试题侧重基础知识的考查,有利于提高学生的分析能力及化学计算能力.

练习册系列答案
相关题目
9.在水溶液中能大量共存的一组离子是( )
| A. | NH4+、K+、Br-、Cl- | B. | Na+、Cu2+、OH-、SO42- | ||
| C. | Mg2+、H+、CH3COO-、SO42- | D. | HCO3-、NO3-、OH-、Na+ |
15.已知一些燃料的燃烧热数据如表:
使用上述燃料,最能体现“低碳经济”理念的是( )
| 燃料 | 甲醇 | 丙烷 | 乙烷 | 乙烯 |
| △H/kJ•mol-1 | -726.0 | -2220.0 | -1560.0 | -1410.0 |
| A. | 甲醇 | B. | 丙烷 | C. | 乙烷 | D. | 乙烯 |
2.含FeS2 A%的黄铁矿ωg,在接触法制硫酸的过程中,损失硫C%,可制得质量分数为B%的硫酸的质量为( )
| A. | $\frac{49ωA(100-C)}{3000B}$g | B. | $\frac{40ω•C%}{30}$g | C. | $\frac{49ωA(1-C%)}{30B}$g | D. | $\frac{30ωA•C%}{49B}$g |
19.下列溶液能用玻璃瓶盛放,但不能用玻璃塞的是( )
| A. | Na2SiO3溶液 | B. | HF溶液 | C. | NaNO3溶液 | D. | NaCl溶液 |
16.下列有关化学术语的表达正确的有( )
①纯碱的分子式为:NaHCO3 ②HCl的电子式: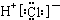
③氟离子的结构示意图: ④过氧化氢的结构式:H-O-O-H
④过氧化氢的结构式:H-O-O-H
⑤苯的最简式:C6H6 ⑥乙烯的结构简式:CH2=CH2.
①纯碱的分子式为:NaHCO3 ②HCl的电子式:
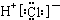
③氟离子的结构示意图:
 ④过氧化氢的结构式:H-O-O-H
④过氧化氢的结构式:H-O-O-H⑤苯的最简式:C6H6 ⑥乙烯的结构简式:CH2=CH2.
| A. | ①②④⑥ | B. | ③④⑥ | C. | ①④⑥ | D. | ④⑥ |
17.下列各组物质中,所含分子数相同的是( )
| A. | 10gH2和10gO2 | B. | 11.2L(标准状况)H2O和0.5molBr2 | ||
| C. | 5.6LN2(标准状况)和11gCO2 | D. | 224mLH2(标准状况)和0.1molN2 |