题目内容
下列离子方程式正确的是( )
| A、稀硫酸与氢氧化钡溶液反应:H++OH-═H2O | ||||
| B、铁与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | ||||
C、实验室制氯气:MnO2+4H++2Cl-
| ||||
| D、向氯化铝溶液滴加少量氨水:Al3++3OH-═Al(OH)3↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.该反应中还生成硫酸钡沉淀;
B.电荷不守恒;
D.二者反应生成氯化锰、水和氯气;
D.弱电解质写化学式.
B.电荷不守恒;
D.二者反应生成氯化锰、水和氯气;
D.弱电解质写化学式.
解答:
解:A.该反应中还生成硫酸钡沉淀,离子方程式为2H++2OH-+SO42-+Ba2+═2H2O+BaSO4↓,故A错误;
B.电荷不守恒,离子方程式为Fe+2Fe3+═3Fe2+,故B错误;
D.二者反应生成氯化锰、水和氯气,离子方程式为MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故C正确;
D.弱电解质写化学式,离子方程式为Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故D错误;
故选C.
B.电荷不守恒,离子方程式为Fe+2Fe3+═3Fe2+,故B错误;
D.二者反应生成氯化锰、水和氯气,离子方程式为MnO2+4H++2Cl-
| ||
D.弱电解质写化学式,离子方程式为Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故D错误;
故选C.
点评:本题考查了离子方程式的书写,明确离子之间发生的反应是解本题关键,再结合离子方程式书写规则书写,要遵循电荷守恒、原子守恒、转移电子守恒,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在2升的密闭容器中,发生以下反应:2A(g)+B(g)?2C(g)+D(g).若最初加入的A和B都是3mol,在前10秒钟A的平均反应速率为0.12mol/(L?s),则10秒钟时,容器中B的物质的量的浓度是( )
| A、1.8mol/L |
| B、1.0mol/L |
| C、0.9mol/L |
| D、2.8mol/L |
如果1g水中含有n个氢原子,则阿伏加德罗常数是( )mol-1.
A、
| ||
| B、9n | ||
| C、2n | ||
| D、n |
向蛋白质中加入下列物质,其中不能使蛋白质失去原有的生理功能的是( )
| A、向蛋白质中加入浓硝酸 |
| B、向蛋白质中加入重金属盐 |
| C、向蛋白质中加入水 |
| D、向蛋白质中加入甲醛 |
下列有机物命名正确的是( )
A、 :2-甲基丁烷 :2-甲基丁烷 |
B、 :2-甲基-1-丙醇 :2-甲基-1-丙醇 |
C、 :甲基苯酚 :甲基苯酚 |
| D、CH2=CH-CH=CH2:1,3-二丁烯 |
下列各数值表示有关元素的原子序数,其中能以共价键相互结合形成稳定化合物的是( )
| A、8与11 | B、9与19 |
| C、2和19 | D、6与8 |
常温下对pH>7的溶液的正确说法是( )
| A、一定是碱溶液 |
| B、一定是强碱弱酸盐的溶液 |
| C、一定是碱性溶液 |
| D、一定是能使酚酞试液变红的溶液 |
在无色透明的溶液中,能大量共存的是( )
A、Na+、N
| ||||
B、H+、C
| ||||
C、K+、S
| ||||
D、Ba2+、Cl-、K+、S
|
下列说法正确的是( )
A、化合物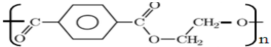 名称为聚对苯甲二酸乙二酯 名称为聚对苯甲二酸乙二酯 |
| B、C3H7OH与C4H9OH分子间脱水,最多可生成6种醚 |
C、1mol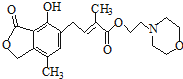 最多可与含4mol NaOH的水溶液完全反应 最多可与含4mol NaOH的水溶液完全反应 |
D、某油脂的化学式为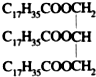 ,它属于酯类但不属于高分子化合物 ,它属于酯类但不属于高分子化合物 |