题目内容
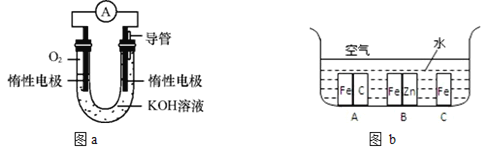
【题目】某实验小组依据甲烷燃烧的反应原理,设计如图a所示的电池装置:
(1)该电池的能量转化形式为____________。
(2)该电池正极的电极反应为____________。
(3)工作一段时间后,测得溶液的pH______,该电池总反应的化学方程式为_________。
(4)在生产生活中,金属腐蚀所带来的损失非常严重,所以防止金属腐蚀已经成为科学研究和技术领域的重大问题。兴趣小组的同学在实验室对金属腐蚀进行了探究。如图b所示,铁处于A、B、C三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)_____。
【答案】(1) 化学能转化为电能(2)O2+2H2O+4e-=4OH-(3)减小 CH4+2O2+2OH-=CO32-+3H2O(4)A>C>B
【解析】
试题(1)该电池的能量转化形式为化学能转化为电能。
(2)原电池中正极得到电子,则氧气在正极通入,其电极反应为O2+2H2O+4e-=4OH-。
(3)由于生成的二氧化碳结合氢氧根转化为碳酸根,则氢氧根浓度减小,因此工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为CH4+2O2+2OH-=CO32-+3H2O。
(4)A处铁与碳形成原电池,铁是负极,加快腐蚀;B处铁与锌构成原电池,锌是负极,铁是正极,被保护,C处是纯铁,发生化学腐蚀,则A、B、C三种不同的环境中,铁被腐蚀的速率由大到小的顺序是A>C>B。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案【题目】下列实验中的颜色变化,与氧化还原反应无关的是
A | B | C | D | |
实验 | NaOH溶液滴入FeSO4溶液中 | 石蕊溶液滴入氯水中 | Na2S溶液滴入AgCl浊液中 | 热铜丝插入稀硝酸中 |
现象 | 产生白色沉淀,随后变为红褐色 | 溶液变红,随后迅速褪色 | 沉淀由白色逐渐变为黑色 | 产生无色气体,随后变为红棕色 |
A. A B. B C. C D. D