题目内容
10.根据化学方程式回答问题:SiO2+2C+2Cl2$\frac{\underline{\;△\;}}{\;}$ SiCl4+2CO①反应中电子转移的数目是4e-.
②在该反应中,还原剂是C.
分析 反应SiO2+2C+2Cl2$\frac{\underline{\;△\;}}{\;}$ SiCl4+2CO中,C元素的化合价升高,Cl元素的化合价降低,结合化合价变化判断反应中电子转移数目及还原剂.
解答 解:反应SiO2+2C+2Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$SiCl4+2CO中,C元素的化合价升高,Cl元素的化合价降低,
(1)C元素的化合价由0升高为+2价,该反应中转移电子为:2×(2-0)=4e-,
故答案为:4e-;
(2)因C元素的化合价升高,则C为还原剂,
故答案为:C.
点评 本题考查氧化还原反应,为高频考点,把握元素的化合价变化为解答的关键,注意掌握氧化还原反应的实质与特征,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
8.下列仪器中一般不能用作反应容器的是( )
| A. | 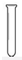 | B. | 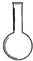 | C. | 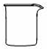 | D. | 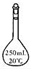 |
1.下列说法不正确的是( )
| A. | 共价键一定存在于共价化合物中,也可能存在于离子化合物中 | |
| B. | Na2O2中既含有离子键也含有极性共价键 | |
| C. | NH4Cl是都由非金属元素组成的既含有离子键也含有共价键的离子化合物 | |
| D. | 熔化状态下不导电的化合物一定是共价化合物 |
18.元素A原子的L电子层比元素B原子的L电子层少3个电子,B元素原子核外电子总数比A元素原子核外电子总数多5个,则A、B形成的化合物的化学式可能为( )
| A. | B2A3 | B. | B3A2 | C. | A2B3 | D. | BA2 |
5.生活中的一些问题常涉及到化学知识,下列叙述正确的是( )
| A. | 晶体硅具有半导体的性质,所以可以制作光导纤维 | |
| B. | 氯化铁溶液可用于制作印刷电路板是因为其具有氧化性,与铜发生置换反应 | |
| C. | 明矾和漂白粉常用于自来水的处理,两者的作用原理相同 | |
| D. | 水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染 |
15.下列有关能源的说法正确的是( )
| A. | 二氧化硅是人类将太阳能转化为电能的常用材料 | |
| B. | 氢氧燃料电池的能量转换率可达100%,是一种具有应用前景的绿色能源 | |
| C. | 设法将太阳光聚焦产生高温,使水分解产生氧气,是开发氢能的研究方向之一 | |
| D. | 原电池是把化学能直接转化为电能的装置,所以由原电池提供的电能是一次能源 |
2.既能与盐酸反应,又能与氢氧化钠溶液反应的化合物是( )
(1)氢氧化铝 (2)三氧化二铝 (3)铝 (4)碳酸氢钠 (5)氢氧化镁.
(1)氢氧化铝 (2)三氧化二铝 (3)铝 (4)碳酸氢钠 (5)氢氧化镁.
| A. | (1)(2)(3)(4) | B. | (1)(2)(3)(4)(5) | C. | (1)(2)(4) | D. | (1)(2)(4)(5) |
19.下列说法正确的是( )
| A. | 6.02×1023就是阿伏加德罗常数 | |
| B. | 1mol Cl2含有2NA个氯原子 | |
| C. | 摩尔既可表示质量,又可以表示数量 | |
| D. | 32g O2所含O2的摩尔数是1mol |
20.据报道,意大利科学家合成了一种新型的氧分子,它是由四个氧原子构成的.下列关于该分子的叙述正确的是( )
| A. | O4的摩尔质量是64 | B. | O2、O3、O4都是氧的同位素 | ||
| C. | O2、O3、O4都是氧的同素异形体 | D. | O2、O3、O4互为同分异构体 |