题目内容
14.下列离子方程式书写正确的是( )| A. | 酸性条件下KIO3溶液与KI溶液发生反应生产I2:IO3-+5I-+3H2O=3I2+6OH- | |
| B. | FeSO4溶液中加入酸性K2Cr2O7溶液:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O | |
| C. | 钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+ | |
| D. | 明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+ |
分析 A.酸性条件下不可能生成OH-;
B.FeSO4溶液中加入酸性K2Cr2O7溶液发生氧化还原反应生成Fe3+和Cr3+;
C.钠和水反应剧烈反应生成氢氧化钠和氢气,应生成氢氧化铜、氢气;
D.生成胶体而不是沉淀.
解答 解:A.酸性条件下不能生成氢氧根离子,原子得守恒,酸性条件下KIO3溶液与KI溶液发生反应生成I2时的离子方程式:IO3-+5I-+6H+═3I2+3H2O,故A错误;
B.FeSO4溶液中加入酸性K2Cr2O7溶液发生氧化还原反应生成Fe3+和Cr3+,反应的离子方程式为6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O,故B正确;
C.钠和水反应剧烈反应生成氢氧化钠和氢气,应生成氢氧化铜、氢气,反应的离子方程式为2Na+2H2O+Cu2+=Cu(OH)2↓+H2↑+2Na+,故C错误;
D.生成胶体而不是沉淀,应为Al3++3H2O=Al(OH)3+3H+,故D错误.
故选B.
点评 本题考查离子反应方程式的书写,明确发生的化学反应及离子反应的书写方法即可解答,B为解答的易错点,注意方程式的书写以及配平,题目难度不大.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
4.已知金属硫化物和溶解性比较复杂,如K2S、Na2S为可溶性硫化物,FeS、ZnS为难溶于水的硫化物,CuS、Ag2S为难溶于水又难溶于强酸的硫化物,下列硫化物和酸的反应不正确的是( )
| A. | Na2S+2HCl=H2S↑+2NaCl | B. | FeSO4+H2S=FeS↓+H2SO4 | ||
| C. | CuSO4+H2S=CuS↓+H2SO4 | D. | ZnS+2HCl=H2S↑+ZnCl2 |
5.下列有关概念的叙述正确的是( )
| A. | 有两种原子构成的物质不一定属于化合物 | |
| B. | 仅含一种元素的物质一定为纯净物 | |
| C. | 既能和酸又能和碱发生反应的氧化物一定为两性氧化物 | |
| D. | 既含有金属元素又含有非金属元素的化合物一定为离子化合物 |
2.3.2g某气态化合物甲在标准状况下的体积为1.12L,则甲的相对分子质量为( )
| A. | 40 g•mol-1 | B. | 22 g•mol-1 | C. | 64 | D. | 22 |
9.下列物质中与CH3C≡CCH3互为同分异构体的是.( )
| A. |  | B. | CH≡CCH3 | C. | CH2=CHCH=CH2 | D. | CH3CH2C≡CCH3 |
19.把碳-12原子质量假设为ng.若某原子质量为wg.则该原子的相对原子质量为( )
| A. | $\frac{12W}{n}$ | B. | $\frac{12n}{W}$ | C. | 6.02×1023W | D. | 12×6.02×1023W |
6.化学科学需要借助化学专用语言来描述.下列有关化学用语正确的是( )
| A. | 质量数为37的氯原子${\;}_{37}^{17}$Cl | B. | 钠原子的电子式 | ||
| C. | 硫原子的结构示意图 | D. | 铝离子的结构示意图 |
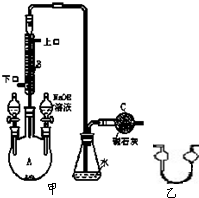 制备溴苯的实验装置如图所示,回答下列问题:
制备溴苯的实验装置如图所示,回答下列问题: 如图是元素周期表中各主族(A)及零族的部分元素符号代码(阴影处为族序数)
如图是元素周期表中各主族(A)及零族的部分元素符号代码(阴影处为族序数)