题目内容
10.下列八种有机物:①CH2=CH2;②CH3CH2COOH;③C2H5OH;④CH3CH2Br;⑤CCl4;⑥CH3COOCH3;⑦CH3COOC2H5;⑧ ,根据官能团的不同可分为( )
,根据官能团的不同可分为( )| A. | 7类 | B. | 6类 | C. | 5类 | D. | 4类 |
分析 ①根据官能团为碳碳双键的烃分析;
②根据官能团为羧基分析;
③根据链烃基与羟基相连分析;
④根据官能团为溴原子判断;
⑤根据官能团为氯原子分析;
⑥根据分子中含有酯基判断;
⑦根据分子中含有酯基分析;
⑧根据羟基直接与苯环相连的结构判断.
解答 解:①CH2═CH2,含有碳碳双键的烃,属于烯烃;
②CH3CH2COOH,分子中含有官能团羧基,属于羧酸;
③C2H5OH,羟基与链烃基相连,属于醇类;
④CH3CH2Br,官能团-Br与烃基相连,属于卤代烃;
⑤CCl4,官能团为-Cl,属于卤代烃;
⑥CH3COOCH3,含有官能团酯基,属于酯类;
⑦CH3COOC2H5,官能团为酯基,属于酯类;
⑧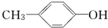 ,官能团羟基与苯环直接相连,属于酚类;
,官能团羟基与苯环直接相连,属于酚类;
所以据官能团的不同可分为:烯烃、羧酸、醇类、卤代烃、酯类和酚类,总共6类,
故选B.
点评 本题考查有机物的简单分类、对官能团的认识等,比较基础,注意醇羟基与酚羟基的区别在于羟基是否直接连接苯环.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
20.一定量的盐酸跟过量的铁粉反应时,为了减慢反应速率,而不影响生成H2的总量,可向其中加入适量的( )
| A. | Na2CO3晶体 | B. | NaOH晶体 | C. | CuSO4溶液 | D. | CH3COONa晶体 |
1.下列有关离子方程式的书写正确的是( )
| A. | 苯酚钠溶液显碱性:C6H5O-+H2O?C6H5OH+OH- | |
| B. | HSO3-在溶液中发生水解:HSO3-+H2O?SO32-+H3O+ | |
| C. | 向Mg(OH)2浊液中滴加FeCl3溶液生成红褐色沉淀:3OH-+Fe3+=Fe(OH)3↓ | |
| D. | 惰性电极电解MgCl2溶液:Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$ OH-+Cl2↑+H2↑ |
18.V、W、X、Y均是元素周期表中短周期元素,在周期表中的相对位置关系如表所示:其中X为常见的金属元素,另有Z为第四周期常见元素,该元素是人体血液中血红蛋白最重要的组成金属元素.V的最简单氢化物为甲,W的最简单氢化物为乙,甲、乙混合时有白烟生成.下列说法正确的是( )
| Y | V | |||
| X | W |
| A. | 少量Z的单质与过量W的单质可化合生成ZW2 | |
| B. | 甲、乙反应的生成物为离子晶体,但其中含有共价键 | |
| C. | 电负性大小关系是:X>Y>V>W | |
| D. | 甲中的V原子杂化类型是sp2 |
5.下列说法正确的是( )
| A. | SO2、H2O、Al均为非电解质 | |
| B. | 以碳做电极,通电后H2SO4完全电离了,并且产生了H2和O2,溶液pH降低 | |
| C. | 由非金属元素构成的物质中一定全部为共价键 | |
| D. | 同主族的元素间也可以构成离子化合物 |
15.某化合物的水溶液能导电,且溶液中不存在电解质分子,但该化合物属于非电解质,符合该条件的物质是( )
| A. | Cl2 | B. | NH3 | C. | SO3 | D. | Na2O |
2.下列物质中不能用化合反应的方法制得的是( )
①SiO2 ②H2SiO3 ③Fe(OH)3 ④Al(OH)3⑤FeSO4 ⑥CaSiO3.
①SiO2 ②H2SiO3 ③Fe(OH)3 ④Al(OH)3⑤FeSO4 ⑥CaSiO3.
| A. | ②④ | B. | ②④⑤ | C. | ②④⑥ | D. | ②③④⑥ |
11.L、M、R、T、W是原子序数依次增大的短周期主族元素,M、T在周期表中的相对位置如表:L与R原子的最外层电子数相同,R的单质是一种常见的半导体材料.请回答下列问题:
(1)T原子的结构示意图为 ,元素W在周期表中位于第三周期第ⅦA族,M单质分子的电子式为
,元素W在周期表中位于第三周期第ⅦA族,M单质分子的电子式为 .
.
(2)R是组成玻璃的元素之一,不能用带磨口玻璃塞的试剂瓶放氢氧化钠溶液的原因是(用化学方程式表示)SiO2+2NaOH═Na2SiO3+H2O.
(3)下列有关相应元素非金属性强弱比较的说法,正确的是(填序号)acd.
a.M的气态氢化物比R的气态氢化物稳定,则非金属性M强于R
b.高温下L的单质能从R的最高价氧化物中置换出R,则非金属性L强于R
c.W的核电荷数比T多,原子半径比T小,得电子能力强,则非金属性W强于T
d.同温、同物质的量浓度的Na2LO3和Na2TO4溶液pH:Na2LO3>Na2TO4,则非金属性T强于L
(4)工业上可用二氧化硅、氯气和焦炭在高温条件下制备RW4,该反应中除RW4外的另一种产物可以用于工业冶炼铁.制备RW4反应的化学方程式为2Cl2+SiO2+2C$\frac{\underline{\;高温\;}}{\;}$SiCl4+2CO.
| M | |
| T |
 ,元素W在周期表中位于第三周期第ⅦA族,M单质分子的电子式为
,元素W在周期表中位于第三周期第ⅦA族,M单质分子的电子式为 .
.(2)R是组成玻璃的元素之一,不能用带磨口玻璃塞的试剂瓶放氢氧化钠溶液的原因是(用化学方程式表示)SiO2+2NaOH═Na2SiO3+H2O.
(3)下列有关相应元素非金属性强弱比较的说法,正确的是(填序号)acd.
a.M的气态氢化物比R的气态氢化物稳定,则非金属性M强于R
b.高温下L的单质能从R的最高价氧化物中置换出R,则非金属性L强于R
c.W的核电荷数比T多,原子半径比T小,得电子能力强,则非金属性W强于T
d.同温、同物质的量浓度的Na2LO3和Na2TO4溶液pH:Na2LO3>Na2TO4,则非金属性T强于L
(4)工业上可用二氧化硅、氯气和焦炭在高温条件下制备RW4,该反应中除RW4外的另一种产物可以用于工业冶炼铁.制备RW4反应的化学方程式为2Cl2+SiO2+2C$\frac{\underline{\;高温\;}}{\;}$SiCl4+2CO.