题目内容
A、B、C、D为四种短周期主族元素,其中A、C同族,B、C同周期,D与A、B不在同周期;A原子最外层电子数是核外电子层数的3倍;B的最高正价与最低负价代数和为6。
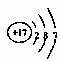
(1)B的原子结构示意图是 ;实验室制备B单质的离子反应方程式是 。
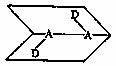
(2)D2A2结构如图所示(两个平面的夹角是93°51′,D―A―A夹角96°52′),D2A2分子属于 (填“极性”或“非极性”)分子。
(3)D2A2溶液与D2C反应生成一种淡黄色的沉淀,该反应的化学方程式是
。
(4)经测定,D2A2为二元弱酸,其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式 。过去常用硫酸处理BaO2来制备D2A2,写出该反应的化学方程式 ;现在实验室可以将过氧化钠加入到水中来制取D2A2,写出该反应的化学方程式 ;简述这两种制备原理的不同之处 。
(1) MnO2+4H++2Cl-
MnO2+4H++2Cl-![]() Mn2++O2↑+2H2O
Mn2++O2↑+2H2O
(2)极性
(3)H2O2+H2S=S↓+2H2O
(4)H2O2![]() H++HO2-,BaO2+H2SO4=BaSO4+H2O2,Na2O2+2H2O=2NaOH+H2O2,前者是酸跟盐反应生成新酸和新盐,利用了强酸制弱酸,后者利用了Na2O2的水解反应。
H++HO2-,BaO2+H2SO4=BaSO4+H2O2,Na2O2+2H2O=2NaOH+H2O2,前者是酸跟盐反应生成新酸和新盐,利用了强酸制弱酸,后者利用了Na2O2的水解反应。

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目

