题目内容
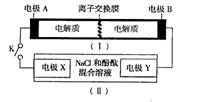
右图装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图.装置(Ⅰ)的离子交换膜只允许Na+ 通过.已知电池充、放电的化学反应方程式为2Na2S2+NaBr3

Na2S4+3NaBr.当闭合开关K时,X极附近溶液变红色.下列说法正确的是( )


Na2S4+3NaBr.当闭合开关K时,X极附近溶液变红色.下列说法正确的是( )
| A.闭合K时,钠离子从右到左通过离子交换膜 |
| B.闭合K时,负极反应为3NaBr-2e-=NaBr3+2Na+ |
| C.闭合K时,X电极的电极反应式为2Cl--2e-=Cl2↑ |
| D.闭合K时,有0.1molNa+通过离子交换膜,X电极上析出标准状况下气体1.12L |

A、原电池中阳离子向正极移动,则闭合K时,钠离子从左到右通过离子交换膜,故A错误;
B、闭合K时,负极发生氧化反应,电极反应为2Na2S2-2e-=2Na++Na2S4,故B错误;
C、闭合K时,X极附近溶液变红色,说明X极生成OH-离子,为电解池的阴极,发生反应为2H2O+2e-=H2↑+2OH-,故C错误;
D、闭合K时,有0.1molNa+通过离子交换膜,说明有0.1mol电子转移,阴极上生成0.05molH2,标准状况下体积为
0.05mol×22.4L/mol=1.12L,故D正确.
故选D.
B、闭合K时,负极发生氧化反应,电极反应为2Na2S2-2e-=2Na++Na2S4,故B错误;
C、闭合K时,X极附近溶液变红色,说明X极生成OH-离子,为电解池的阴极,发生反应为2H2O+2e-=H2↑+2OH-,故C错误;
D、闭合K时,有0.1molNa+通过离子交换膜,说明有0.1mol电子转移,阴极上生成0.05molH2,标准状况下体积为
0.05mol×22.4L/mol=1.12L,故D正确.
故选D.

练习册系列答案
相关题目
如图装置(I)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池放电、充电的化学方程式为:2K2S2+KI3  K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是 ( )
K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是 ( )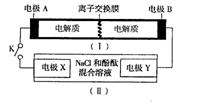
| A.K+从右到左通过离子交换膜 |
| B.电极A上发生的反应为:3I--2e-=I3- |
| C.电极X上发生的反应为:2Cl--2e-=C12↑ |
| D.当有0.1 mol K+通过离子交换膜,X电极上产生1.12 L气体(标准状况) |
 K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是 ( )
K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是 ( )