题目内容
有一杯红褐色的透明液体,它可能是Fe(OH)3溶胶,为了证明它不是溶液而是胶体,可采用的最简单方法是( )
| A、丁达尔实验 | B、加入盐酸 |
| C、加热 | D、静置 |
考点:分散系、胶体与溶液的概念及关系
专题:溶液和胶体专题
分析:溶液和胶体均属于分散系,外观都是透明的红褐色的液体,但是胶体具有丁达尔效应,当可见光入射时,会产生光亮的通路,丁达尔效应是胶体特有的性质,常用来区别胶体与溶液.
解答:
解:胶体具有丁达尔效应,溶液不具有,所以可以借助丁达尔效应判断溶液和胶体,
故选:A.
故选:A.
点评:本题考查了胶体的性质,明确丁达尔效应是胶体特有的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
在FeCl3和CuCl2的混合溶液中加入铁屑,反应结束后滤出固体物质,滤液中的阳离子可能是 ( )
①只有Fe2+;
②Fe2+和Fe3+;
③Fe2+和Cu2+;
④Cu2+和Fe3+.
①只有Fe2+;
②Fe2+和Fe3+;
③Fe2+和Cu2+;
④Cu2+和Fe3+.
| A、①③ | B、②④ | C、①④ | D、②③ |
下列物质不是配合物的是( )
| A、NH4Cl |
| B、KAl(SO4)2?12H2O |
| C、CuSO4?5H2O |
| D、[Ag(NH3)2]OH |
将小苏打和十水碳酸钠的混合物10.0g溶于水制成200mL溶液,其中c(Na+)=0.5mol/L,若将10.0g该混合物加热到恒重,混合物会失重( )
| A、3.0g | B、4g |
| C、4.7g | D、5g |
以下关于金属的金属性的判断正确的是( )
| A、镁和铝与同浓度的盐酸反应铝没镁反应剧烈,所以铝比镁的金属性强 |
| B、Mg(OH)2溶液的碱性比NaOH溶液的碱性弱,所以镁比钠的金属性强 |
| C、铁能从CuSO4溶液中置换出铜,所以铁比铜的金属性强 |
| D、电解含Ag+和Cu2+的溶液时,Ag+优先放电,所以银比铜的金属性强 |
下列说法正确的是( )
| A、海水中提取镁的过程中有用到硫酸 |
| B、工业炼铁中加入石灰石的目的是除去铁矿石中的杂质 |
| C、铁、铝常温下不能和浓硫酸、浓硝酸反应 |
| D、铝热反应特指铝与氧化铁的反应 |
短周期元素W、X、Y、Z的原子序数依次增大,W与Y原子的最外层电子数之和为X原子的最外层电子数的2倍,Z原子的最外层电子数等于其最内层电子数,X、Y、Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体.下列说法正确的是( )
| A、元素Y的气态氢化物比W的稳定 |
| B、元素Y的最高正价与负价绝对值的和等于8 |
| C、化合物XY2与ZY2分子中的化学键类型相同 |
| D、原子半径的大小顺序:r(W)>r(X)>r(Y)>r(Z) |
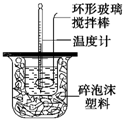 在量热器中将50ml、0.50mol?L-1CH3COOH溶液与50ml、0.55mol?L-1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J?0C-1,C=4.18J?g-1?0C-1,溶液的密度为1g?cm-3.
在量热器中将50ml、0.50mol?L-1CH3COOH溶液与50ml、0.55mol?L-1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J?0C-1,C=4.18J?g-1?0C-1,溶液的密度为1g?cm-3. 液,试画出原电池的装置图,并说明其工作原理.
液,试画出原电池的装置图,并说明其工作原理.