题目内容
在恒温恒容容器中进行反应A(g) 2B(g)+C(g),若A的浓度由0.1 mol·L
2B(g)+C(g),若A的浓度由0.1 mol·L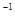 降到0.06 mol·L
降到0.06 mol·L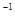 需20 s,那么由0.06 mol·L
需20 s,那么由0.06 mol·L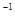 降到0.024 mol·L
降到0.024 mol·L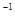 需要的时间
需要的时间
A.等于18s B,等于12s C,小于18s D.大于18s
 2B(g)+C(g),若A的浓度由0.1 mol·L
2B(g)+C(g),若A的浓度由0.1 mol·L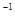 降到0.06 mol·L
降到0.06 mol·L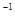 需20 s,那么由0.06 mol·L
需20 s,那么由0.06 mol·L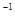 降到0.024 mol·L
降到0.024 mol·L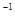 需要的时间
需要的时间A.等于18s B,等于12s C,小于18s D.大于18s
D
试题分析:前20s的平均速率是(0.1-0.06) mol·L
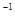 /20s=0.002 mol·L
/20s=0.002 mol·L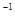 ·s
·s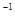 。按这种平均速率计算,0.06 mol·L
。按这种平均速率计算,0.06 mol·L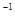 降到0.024 mol·L
降到0.024 mol·L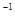 需要的时间(0/06-0.024) mol·L
需要的时间(0/06-0.024) mol·L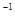 /0.002 mol·L
/0.002 mol·L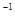 ·s
·s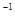 =18s,由于反应的进行,A的浓度越来越小,故所需时间要大于18s。
=18s,由于反应的进行,A的浓度越来越小,故所需时间要大于18s。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 ?pC(g)+2D(g),生成0.5 mol D,又知C的平均反应速率是0.1 mol/(L·s),则下列说法中正确的是
?pC(g)+2D(g),生成0.5 mol D,又知C的平均反应速率是0.1 mol/(L·s),则下列说法中正确的是 实验测得不同温度下的平衡数据列于下表:
实验测得不同温度下的平衡数据列于下表:
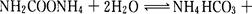
 该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到C(NH2C00-)随时间的变化趋势如图所示。
该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到C(NH2C00-)随时间的变化趋势如图所示。
 M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表: