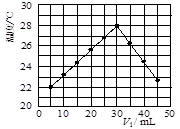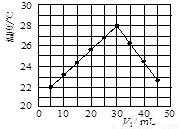��Ŀ����
 ij�о�С�齫V1 mL 1.0mol/L HCl��Һ��V2 mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ������ͼ��ʾ��ʵ����ʼ�ձ���V1+V2=50mL�����ش��������⣺
ij�о�С�齫V1 mL 1.0mol/L HCl��Һ��V2 mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ������ͼ��ʾ��ʵ����ʼ�ձ���V1+V2=50mL�����ش��������⣺��1���о�С������ʵ��ʱ�����¶�
����
����
������ڡ��������ڡ����ڡ���22�棬�жϵ�������5mLHCl��Һ��45mLNaOH��Һ��Ӧ���Ⱥ���¶��Ѿ���22�棬����Һ���ǰ��ʵ�黷���¶�һ������22��
5mLHCl��Һ��45mLNaOH��Һ��Ӧ���Ⱥ���¶��Ѿ���22�棬����Һ���ǰ��ʵ�黷���¶�һ������22��
����2������ɼ�ͼ�ο�֪��V1��V2=
3��2
3��2
ʱ�����ǡ����ȫ�кͣ��˷�Ӧ����NaOH��Һ��Ũ��ӦΪ1.5
1.5
mol/L����3��ʵ��ʱ������ڼ������ȼ��л�ϣ�����
����������
����������
���裬ʹ��Һ��Ͼ��ȣ����йؼ���֪�˷�Ӧ���ų�Q kJ����������д���˷�Ӧ���Ȼ�ѧ����ʽ��H+��aq��+OH-��aq��=H2O��l����H=-
kJ?mol-1��HCl��aq��+NaOH��aq��=NaCl��aq��+H2O��l����H=-
kJ?mol-1��
| 100Q |
| 3 |
| 100Q |
| 3 |
H+��aq��+OH-��aq��=H2O��l����H=-
kJ?mol-1��HCl��aq��+NaOH��aq��=NaCl��aq��+H2O��l����H=-
kJ?mol-1��
��| 100Q |
| 3 |
| 100Q |
| 3 |
��������1����ͼʾ�۲����ʼ�¶ȼ�Ϊʵ��ʱ���¶ȣ�
��2����ͼ��֪��ǡ�÷�Ӧʱ�μӷ�Ӧ��������Һ�������30mL����V1+V2=50mL��֪�����ĵ�����������Һ�����Ϊ20mL���Դ�������ߵ������ֵ������NaOHŨ�ȣ�
��3��Ϊʹ�����ȫ��Ӧ��Ӧ�û��β�������������ݡ�H=-
�������H�����ݻ�ѧ�������͡�H��ϵд���Ȼ�ѧ����ʽ��
��2����ͼ��֪��ǡ�÷�Ӧʱ�μӷ�Ӧ��������Һ�������30mL����V1+V2=50mL��֪�����ĵ�����������Һ�����Ϊ20mL���Դ�������ߵ������ֵ������NaOHŨ�ȣ�
��3��Ϊʹ�����ȫ��Ӧ��Ӧ�û��β�������������ݡ�H=-
| Q |
| n |
����⣺��1������ʵ����ͼ2��ʾ��5mLHCl��Һ��45mLNaOH��Һ��Ӧ���Ⱥ���¶��Ѿ���22�棬����֪����ʵ�鿪ʼʱ�¶�һ���ǵ���22�棬
�ʴ�Ϊ�����ڣ�5mLHCl��Һ��45mLNaOH��Һ��Ӧ���Ⱥ���¶��Ѿ���22�棬����Һ���ǰ��ʵ�黷���¶�һ������22�棻
��2��ǡ�÷�Ӧʱ�μӷ�Ӧ��������Һ�������30mL����V1+V2=50mL�����ĵ�����������Һ�����Ϊ20mL������V1/V2=3/2����ǡ�÷�Ӧʱ����������Һ�����ʵ����ʵ���Ϊn��
HCl+NaOH�TNaCl+H2O
1 1
1.0mol?L-1��0.03L n
��n=1.0mol?L-1��0.03L=0.03mol��
����Ũ��C=
=1.5mol/L��
�ʴ�Ϊ��3��2��1.5��
��3��Ϊʹ�����ȫ��Ӧ��Ӧ�û��β����������
20mL 1.5mol/L����������30mL 1.0mol/L������Һ�����кͷ�Ӧ����ˮ�����ʵ���Ϊ0.02L��1.50mol/L=0.03mol����H=-
KJ/mol=-
KJ/mol����Ӧ���Ȼ�ѧ����ʽΪ��H+��aq��+OH-��aq��=H2O ��l����H=-
kJ?mol-1��HCl��aq��+NaOH��aq��=NaCl��aq��+H2O ��l����H=-
kJ?mol-1��
�ʴ�Ϊ�����β����������H+��aq��+OH-��aq��=H2O��l����H=-
kJ?mol-1��HCl��aq��+NaOH��aq��=NaCl��aq��+H2O��l����H=-
kJ?mol-1��
�ʴ�Ϊ�����ڣ�5mLHCl��Һ��45mLNaOH��Һ��Ӧ���Ⱥ���¶��Ѿ���22�棬����Һ���ǰ��ʵ�黷���¶�һ������22�棻
��2��ǡ�÷�Ӧʱ�μӷ�Ӧ��������Һ�������30mL����V1+V2=50mL�����ĵ�����������Һ�����Ϊ20mL������V1/V2=3/2����ǡ�÷�Ӧʱ����������Һ�����ʵ����ʵ���Ϊn��
HCl+NaOH�TNaCl+H2O
1 1
1.0mol?L-1��0.03L n
��n=1.0mol?L-1��0.03L=0.03mol��
����Ũ��C=
| 0.03mol |
| 0.02L |
�ʴ�Ϊ��3��2��1.5��
��3��Ϊʹ�����ȫ��Ӧ��Ӧ�û��β����������
20mL 1.5mol/L����������30mL 1.0mol/L������Һ�����кͷ�Ӧ����ˮ�����ʵ���Ϊ0.02L��1.50mol/L=0.03mol����H=-
| Q |
| 0.03 |
| 100Q |
| 3 |
| 100Q |
| 3 |
| 100Q |
| 3 |
�ʴ�Ϊ�����β����������H+��aq��+OH-��aq��=H2O��l����H=-
| 100Q |
| 3 |
| 100Q |
| 3 |
���������⿼�����к��ȵļ������⣬ע���ͼʾ�ó�������Ϣ�ǽ����Ĺؼ�����ע���к��ȵ��ȷ���ʽ����д���������

��ϰ��ϵ�д�
�����Ŀ
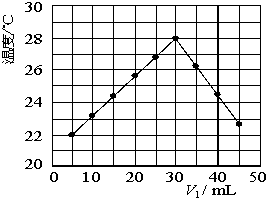 ij�о�С�齫V1 mL 1.0mol/L HCl��Һ��V2 mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ��������ͼ��ʾ��ʵ����ʼ�ձ���V1+V2=50mL�����ش��������⣺
ij�о�С�齫V1 mL 1.0mol/L HCl��Һ��V2 mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ��������ͼ��ʾ��ʵ����ʼ�ձ���V1+V2=50mL�����ش��������⣺