题目内容
(10分)在10mL含有AlO2-离子的溶液中逐滴加入1mol/L的盐酸,所得Al(OH)3沉淀质量和所加盐酸的体积关系如图所示。
问:(1)此溶液中除含有AlO2- 外,还同时含有_ ___mol__ _ 离子;
(2)用离子方程式表示MN段发生的反应是
(3)原溶液中,c (AlO2-) 是 mol/L
(4)加盐酸到点N处,滴入的HCl溶液体积共为 ml
(1)0.02mol;OH- (2) 
(3)1 (4)60ml
解析试题分析:(1)在A处开始产生沉淀,此前共消耗20ml的盐酸,即0.02mol的盐酸,由于溶液显碱性,则含有OH-,共0.02mol;
(2)图中MN段表示 与盐酸的反应;
与盐酸的反应;
AlO2-离子完全生成沉淀共消耗10ml盐酸,根据 可计算得c (AlO2-) 是1mol/L;
可计算得c (AlO2-) 是1mol/L;
(4)AlO2-物质的量为0.01mol,则Al(OH)3物质的量为0.01mol则BN段消耗的盐酸为0.03mol,体积为0.03mol/1mol/L=0.03L即30mL,所以加盐酸到点N处,滴入的HCl溶液体积共为60mL。
考点:铝的化合物的性质
点评:本题考查铝的化合物的性质,主要考查了AlO2-离子的溶液与盐酸反应的计算,根据所给的关系图以及化学反应方程式,则不难计算。

练习册系列答案
相关题目
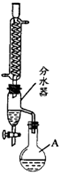 (2012?江苏三模)乙酸正丁酯是常用的食用香精.实验室用正丁醇和乙酸制备乙酸正丁酯的装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下:
(2012?江苏三模)乙酸正丁酯是常用的食用香精.实验室用正丁醇和乙酸制备乙酸正丁酯的装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下: 时间之后,又可以观察到的现象是 。试解释易拉罐变瘪的原因 ;并解释后一现象的原因 。写出反应过程中的两个离子方程式 ; 。
时间之后,又可以观察到的现象是 。试解释易拉罐变瘪的原因 ;并解释后一现象的原因 。写出反应过程中的两个离子方程式 ; 。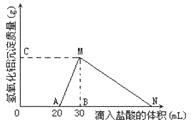
 罐中收集满CO2,然后倒入10mL浓NaO
罐中收集满CO2,然后倒入10mL浓NaO H溶液,迅速密封易拉罐口,可以观察到易拉罐突然变瘪了,原因是 _____________________,反应的离子方程式为 ___________________。
H溶液,迅速密封易拉罐口,可以观察到易拉罐突然变瘪了,原因是 _____________________,反应的离子方程式为 ___________________。