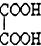题目内容
12.现有易溶于水的五种物质A、B、C、D、E,其中有一种是碱,四种是盐,溶于水后电离可以产生下表中的离子:| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO32- SO42- |
①A溶液与B溶液反应生成无色气体x,x可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成自色沉淀D,沉淀D不溶于稀硝酸.
请根据上述实验结果,填空:
(1)写出下列物质的化学式:XCO2,CBa(OH)2,BNaHSO4
(2)完成A溶液与X 气体反应的离子方程式:CO32-+H2O+CO2=2HCO3-
(3)D 与E的混介物ag,加入足量盐酸,反应完毕生成标准状况时的气体bL,则D在混合物中的质量分数为1-$\frac{197b}{22.4a}$×100%.
(4)已知NaHCO3溶液呈碱性.B 溶液与A 溶液反应至恰好溶液呈中性,写出该过程的离子反应方程式2H++CO32-=H2O+CO2↑.
分析 生成的气体只有CO2符合,发生的反应为 2H++CO32-=H2O+CO2↑,CO2气体可以和C溶液反应生成沉淀D,则C为Ba(OH)2,沉淀E为BaCO3,与B溶液反应,则B为NaHSO4,所以A为Na2CO3,沉淀D为BaSO4,根据物质的性质和反应的有关方程式解答该题;
解答 解:生成的气体只有CO2符合,发生的反应为 2H++CO32-=H2O+CO2↑,CO2气体可以和C溶液反应生成沉淀D,则C为Ba(OH)2,沉淀D为BaCO3,与B溶液反应,则B为NaHSO4,所以A为Na2CO3;
(1)生成的气体只有CO2符合,发生的反应为 2H++CO32-=H2O+CO2↑,结合分析可知C为Ba(OH)2,B为NaHSO4,故答案为:CO2; Ba(OH)2;NaHSO4;
(2)A为Na2CO3溶液,通入CO2发生反应的化学方程式为Na2CO3+H2O+CO2=2NaHCO3,改写为离子方程式得CO32-+H2O+CO2=2HCO3-,故答案为:CO32-+H2O+CO2=2HCO3-;
(3)碳酸钡和硫酸钡的混合物中滴加盐酸,只有碳酸钡溶解并生成CO2气体,根据原子守恒,n(BaCO3)=n(CO2)=bL÷22.4L/mol=$\frac{b}{22.4}$mol,碳酸钡在混合物中的质量分数为$\frac{\frac{b}{22.4}mol×197g/mol}{a}×100%$=$\frac{197b}{22.4a}$×100%,D物质硫酸钡的质量分数为1-$\frac{197b}{22.4a}$×100%,故答案为:1-$\frac{197b}{22.4a}$×100%;
(4)碳酸钠溶液与硫酸氢钠溶液反应可能生成碳酸氢钠,也可以生成CO2气体,同时得到硫酸钠溶液,硫酸钠溶液显中性,故反应的离子方程式为2H++CO32-=H2O+CO2↑,故答案为:2H++CO32-=H2O+CO2↑.
点评 本题考查较为综合,涉及离子方程式的书写,离子的检验以及含量的计算,题目难度中等,注意根据物质的性质判断物质的成分为解答该题的关键.

| A. | 混合气体的颜色不再改变 | |
| B. | 混合气体的密度不再改变 | |
| C. | 混合气体的压强不再改变 | |
| D. | 混合气体的平均相对分子质量不再改变 |
| A. | 36g水中含有的水分子数是2NA | |
| B. | 标准状况下,33.6LCO中含有的原子数是3NA | |
| C. | 0.5L0.2mol/L的NaCl溶液中含有的Na+数是0.1NA | |
| D. | 常温常压下,1molCH4的体积约为22.4L |
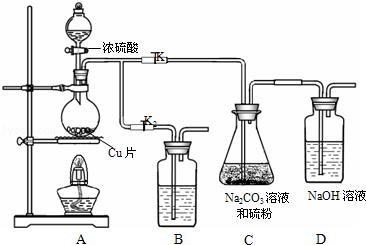
已知:Na2S2O3在酸性溶液中不能稳定存在.
(1)某研究小组设计了制备Na2S2O3•5H2O的装置和部分操作步骤如下.
步骤1:如图连接后装置后,打开K1,关闭K2,将D中导管末端浸入水中,微热烧瓶观察气泡和水柱,检查装置A、C、D气密性;
步骤2:加入药品,打开K1,关闭K2,向圆底烧瓶中加入足量浓硫酸,加热;
装置B中的药品可选用下列物质中的AC
A.NaOH溶液 B.浓H2SO4 C.酸性KMnO4溶液 D饱和NaHSO3溶液
步骤3:C中的混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当C中溶液的pH接近7时打开K2,关闭K1即停止C中的反应,停止加热.“当C中溶液的pH接近7时即停止C中的反应”的原因是S2O32-+2H+═S↓+H2O+SO2↑.(用离子方程式表示)
步骤4:过滤C中的混合液,将滤液经过加热浓缩,趁热过滤,再将滤液冷却结晶、过滤、洗涤、烘干,得到产品
(2)Na2S2O3性质的检验,向足量的新制氯水中滴加少量的Na2S2O3溶液,氯水颜色变浅,检查反应后的溶液中有硫酸根,写出该反应的离子方程式S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+;
(3)常用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解.此时CrO42-全部转化为Cr2O72-;再加过量KI溶液,充分反应后,得到混合溶液Vml,将其分成4等分,加入淀粉溶液作指示剂,用0.010mol•L-1的Na2S2O3溶液进行滴定,相关数据如表所示
| 编 号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
判断达到滴定终点的现象是当滴入最后一滴Na2S2O3时,溶液蓝色消失且半分钟不变色.
废水中Ba2+的物质的量浓度为0.0024mol/L.
| A. | KMnO4→K2MnO4 | B. | HCl→Cl2 | C. | Fe3+→Fe2+ | D. | Na2O→NaOH |