题目内容
7.一定温度下,有某一元弱酸HA,一元强酸HB,二元强酸H2C,回答下列问题:①当上述三者物质的量浓度相同时,pH值由大到小顺序为HA>HB>H2C;
②同体积、同物质的量浓度的三种酸,中和氢氧化钠的能力由大到小顺序为H2C>HA=HB;
③pH相同、体积相同的三种溶液分别与足量Zn反应,相同状况下生成H2体积由大到小顺序为HA>HB=H2C.
分析 ①强电解质完全电离,弱电解质部分电离,c(H+)越大该溶液pH越小;
②同体积、同物质的量浓度的三种酸,其物质的量相等,中和NaOH能力与最终电离出n(H+)成正比;
③pH相同体积相同的三种溶液分别与足量Zn反应生成相同状况下氢气体积与最终电离出n(H+)成正比.
解答 解:①强电解质完全电离,弱电解质部分电离,c(H+)越大该溶液pH越小,一元弱酸HA,一元强酸HB,二元强酸H2C,三种溶液物质的量浓度相同时,c(H+)从小到大顺序是HA>HB>H2C,所以pH大小顺序是HA>HB>H2C,故答案为:HA>HB>H2C;
②同体积、同物质的量浓度的三种酸,其物质的量相等,中和NaOH能力与最终电离出n(H+)成正比,一元弱酸HA,一元强酸HB,二元强酸H2C,最终电离出n(H+)从小到大顺序是HA=HB<H2C,则中和氢氧化钠的能力由大到小顺序为H2C>HA=HB,故答案为:H2C>HA=HB;
③pH相同体积相同的三种溶液分别与足量Zn反应生成相同状况下氢气体积与最终电离出n(H+)成正比,一元弱酸HA,一元强酸HB,二元强酸H2C,pH相同、体积相同的三种溶液最终电离出n(H+)大小顺序是HA>HB=H2C,所以相同状况下生成H2体积由大到小顺序为HA>HB=H2C,故答案为:HA>HB=H2C.
点评 本题考查弱电解质的电离,为高频考点,明确各个物理量之间关系是解本题关键,注意中和碱能力与酸的强弱无关,只与酸最终电离出n(H+)有关,题目难度不大.

练习册系列答案
相关题目
18.新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化.某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式如图,下列说法正确的是( )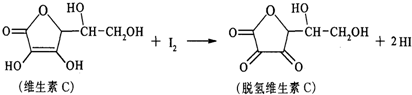

| A. | 上述反应为取代反应 | |
| B. | 维生素C能使高锰酸钾酸性溶液褪色 | |
| C. | 维生素C不溶于水,可溶于有机溶剂 | |
| D. | 维生素C的分子式为C6H10O6 |
2.对于下列反应的反应类型的判断,不正确的是( )
| A. | CO2+H2O═H2CO3化合反应 | |
| B. | Cu2(OH)2CO3═2CuO+H2O+CO2↑ 分解反应 | |
| C. | CuO+CO═Cu+CO2 置换反应 | |
| D. | NaCl+AgNO3═AgCl↓+NaNO3复分解反应 |
19.下列离子方程式不正确的是( )
| A. | 向烧碱液中通入过量的二氧化碳:2OH-+CO2═CO32-+H2O | |
| B. | 向纯碱溶液通入足量的二氧化碳:CO32-+CO2+H2O═2HCO3- | |
| C. | 向硅酸钠水液中通人少量的二氧化碳:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| D. | 向次氯酸钠溶液中通人少量的二氧化碳:ClO-+CO2+H2O═HClO+HCO3- |
12.现有易溶于水的五种物质A、B、C、D、E,其中有一种是碱,四种是盐,溶于水后电离可以产生下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体x,x可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成自色沉淀D,沉淀D不溶于稀硝酸.
请根据上述实验结果,填空:
(1)写出下列物质的化学式:XCO2,CBa(OH)2,BNaHSO4
(2)完成A溶液与X 气体反应的离子方程式:CO32-+H2O+CO2=2HCO3-
(3)D 与E的混介物ag,加入足量盐酸,反应完毕生成标准状况时的气体bL,则D在混合物中的质量分数为1-$\frac{197b}{22.4a}$×100%.
(4)已知NaHCO3溶液呈碱性.B 溶液与A 溶液反应至恰好溶液呈中性,写出该过程的离子反应方程式2H++CO32-=H2O+CO2↑.
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO32- SO42- |
①A溶液与B溶液反应生成无色气体x,x可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成自色沉淀D,沉淀D不溶于稀硝酸.
请根据上述实验结果,填空:
(1)写出下列物质的化学式:XCO2,CBa(OH)2,BNaHSO4
(2)完成A溶液与X 气体反应的离子方程式:CO32-+H2O+CO2=2HCO3-
(3)D 与E的混介物ag,加入足量盐酸,反应完毕生成标准状况时的气体bL,则D在混合物中的质量分数为1-$\frac{197b}{22.4a}$×100%.
(4)已知NaHCO3溶液呈碱性.B 溶液与A 溶液反应至恰好溶液呈中性,写出该过程的离子反应方程式2H++CO32-=H2O+CO2↑.
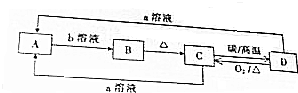
 .D燃烧放出大量热量,有望成为二十一世纪的新能源,与“传统能源”相比,它具有便于储运,比较安全(写出两点)等更加优越的特点.
.D燃烧放出大量热量,有望成为二十一世纪的新能源,与“传统能源”相比,它具有便于储运,比较安全(写出两点)等更加优越的特点.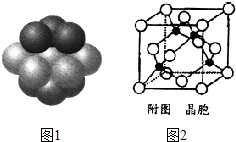 铁和铜都是日常生活中常见的金属,有着广泛的用途.请回答下列问题:
铁和铜都是日常生活中常见的金属,有着广泛的用途.请回答下列问题: