题目内容
18.许多化学反应都能生成水.请按照以下反应类型,各写一个生成水的化学方程式:(1)化合反应2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(2)分解反应H2CO3=H2O+CO2↑ _;
(3)置换反应H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$H2O+Cu;
(4)复分解反应HCl+NaOH=NaCl+H2O;
并判断你写出来的方程式中哪些是属于氧化还原反应(写序号)(1)(3).
分析 (1)化合反应:两种或两种以上的物质反应后生成一种新物质的反应.(多变一) A+B=AB;如氢气点燃生成水;
(2)分解反应:由一种物质生成两种或两种以上其他物质的反应.(一变多)AB=A+B;如碳酸分解或胆矾分解;
(3)置换反应:一种单质和一种化合物反应生成另一种的单质和另一种的化合物的反应;(单质+化合物=单质+化合物)即 A+BC=B+AC;如氢气还原氧化铁或氧化铜的反应;
(4)复分解反应:由两种化合物互相交换成分,生成另外两种化合物的反应:(AB+CD=AD+CB);
氧化还原反应判断依据:有化合价变化的反应.
解答 解:(1)2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,反应中有化合价变化,属于氧化还原反应;
故答案为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(2)H2CO3=H2O+CO2↑,反应中没有化合价变化,不属于氧化还原反应;
故答案为:H2CO3=H2O+CO2↑;
(3)H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$H2O+Cu,反应中有化合价变化,属于氧化还原反应;
故答案为:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$H2O+Cu;
(4)HCl+NaOH=NaCl+H2O,反应中没有化合价变化,不属于氧化还原反应;
故答案为:HCl+NaOH=NaCl+H2O;
所以属于氧化还原反应的为:(1)(3);
故答案为:(1)(3).
点评 本题考查了四种基本反应类型、氧化还原反应定义,方程式书写,掌握反应类型的判定方法、各自反应特点是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.德班气候大会上,各国就减排承诺展开讨论.减排主要是指减少下列哪种气体的排放量( )
| A. | 二氧化碳 | B. | 二氧化硫 | C. | 氮氧化物 | D. | 氟氯烃 |
6.将Na2O2投入FeCl3溶液中,可观察到的现象是( )
| A. | 生成白色沉淀 | B. | 只生成红褐色沉淀 | ||
| C. | 有气泡产生,同时生成红褐色沉淀 | D. | 无变化 |
10.下列表示物质结构的化学用语或模型正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | CH4分子的比例模型: | ||
| C. | 羟基的电子式: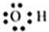 | D. | CCl4的电子式: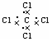 |
7.下列化学实验事实及其结论都正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO的氧化性比H2SO4强 |
| B | 向溶液X中先滴加稀硝酸,再滴加BaCl2,出现白色沉淀 | 溶液X中一定含有SO42- |
| C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化物 |
| D | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
8.下列叙述正确的是( )
| A. | 在水玻璃中通入过量二氧化碳,加热蒸干,最终得到混合物 | |
| B. | 铁件镀铜的目的是利用电化学防腐原理保护铁件不受腐蚀 | |
| C. | 制糖工业用活性炭脱色和制纸工业用次氯酸盐漂白纸浆的原理相同 | |
| D. | 使红色石蕊试纸变蓝的溶液中能大显存在Na+、Fe3+、NO3-、Cl- |



