题目内容
0.1mol 某烃完全燃烧生成的产物全部通过足量的碱石灰,使碱石灰增重44.2g.在120℃和相同压强下,测得生成的CO2的体积是H2O(气)体积的1.6倍,已知该烃不能使溴水褪色,可使KMnO4酸性溶液褪色.则该烃的分子式为 ,写出其可能的结构简式: 、 、 、 .
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:0.1mol某烃完全燃烧生成的产物全部通过足量的碱石灰,使碱石灰增重44.2g,即H2O和CO2的总质量为44.2g,在120℃和相同压强下,生成的CO2的体积是H2O(气)体积的1.6倍,设H2O的物质的量为xmol,则CO2的物质的量为1.6xmol,根据题意有18x+44×1.6x=44.2,解得x=0.5,即H2O的物质的量为0.5mol,所以CO2的物质的量为0.8mol,根据元素守恒可知,该物质化学式为C8H10,该烃不能使溴水褪色,说明不含碳碳双键或碳碳参键,可使KMnO4酸性溶液褪色,说明该物质为苯的同系物,据此答题.
解答:
解:0.1mol某烃完全燃烧生成的产物全部通过足量的碱石灰,使碱石灰增重44.2g,碱石灰增重为H2O和CO2,总质量为44.2g,
在120℃和相同压强下,生成的CO2的体积是H2O(气)体积的1.6倍,设H2O的物质的量为xmol,则CO2的物质的量为1.6xmol,则:18x+44×1.6x=44.2,解得:x=0.5,
即:H2O的物质的量为0.5mol,所以CO2的物质的量为0.8mol,
根据元素守恒可知,该有机物分子中含有C、H原子数为:N(C)=
=8、N(H)=
=10,
所以该物质化学式为C8H10;
该烃不能使溴水褪色,说明不含碳碳双键或碳碳参键,可使KMnO4酸性溶液褪色,说明该物质为苯的同系物,所以可推知该烃的结构简式可能为: 、
、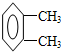 、
、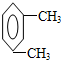 、
、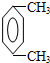 ,
,
故答案为:C8H10; ;
; ;
; ;
; .
.
在120℃和相同压强下,生成的CO2的体积是H2O(气)体积的1.6倍,设H2O的物质的量为xmol,则CO2的物质的量为1.6xmol,则:18x+44×1.6x=44.2,解得:x=0.5,
即:H2O的物质的量为0.5mol,所以CO2的物质的量为0.8mol,
根据元素守恒可知,该有机物分子中含有C、H原子数为:N(C)=
| 0.8mol |
| 0.1mol |
| 0.5mol×2 |
| 0.1mol |
所以该物质化学式为C8H10;
该烃不能使溴水褪色,说明不含碳碳双键或碳碳参键,可使KMnO4酸性溶液褪色,说明该物质为苯的同系物,所以可推知该烃的结构简式可能为:
 、
、 、
、 、
、 ,
,故答案为:C8H10;
 ;
; ;
; ;
; .
.
点评:本题考查了有机物分子式、结构简式的确定,题目难度中等,明确苯及其同系物的性质为解答关键,注意掌握质量守恒在确定有机物分子式中的应用方法.

练习册系列答案
相关题目
下列对化学反应的认识错误的是( )
| A、一定会发生电子转移 |
| B、有旧键断裂和新键的形成 |
| C、原子一定发生重新组合 |
| D、必然伴随着能量的变化 |
某锂电池的电池总反应为4Li+2SOCl2=4LiCl+S+SO2,下列有关说法正确的是( )
| A、锂电极作电池负极,放电过程中发生还原反应 |
| B、1 mol SOCl2发生电极反应转移的电子数为4 mol |
| C、电池的正极反应为2SOCl2+2e-=4Cl-+S+SO2 |
| D、组装该电池必须在无水、无氧的条件下进行 |
下列说法正确的是( )
| A、乙烯和聚乙烯的元素组成相同,性质相似,如均能使溴水褪色 |
| B、CH3-CH═CH-CH3与C3H6互为同系物 |
C、 的名称是2,3-二甲基丁烷 的名称是2,3-二甲基丁烷 |
| D、乙醇可与水以任意比例混溶,是因为与水形成了氢键 |
有三个组成均为CrCl3?6H2O的配合物,甲为亮绿色,乙为暗绿色,丙为紫色,相同物质的量的甲、乙、丙的水溶液中加入足量的AgNO3溶液,析出AgCl的物质的量之比分别为2:1:3.已知铬的配位数为6,下列说法正确的是( )
| A、甲、乙、丙为同一物质 |
| B、配体均为Cl- |
| C、铬元素均显+3价 |
| D、甲的化学式为[Cr(H2O)6]Cl3 |
下列物质中属于酚类,且是苯酚的同系物的是( )
A、 |
B、 |
C、 |
D、 |

 在酸性条件下生成氯吡格雷和另一种常见有机物,试写出该反应的化学方程式.
在酸性条件下生成氯吡格雷和另一种常见有机物,试写出该反应的化学方程式.
 的合成路线流程图(无机试剂任选).合成路线流程示意图为:CH3CH2OH
的合成路线流程图(无机试剂任选).合成路线流程示意图为:CH3CH2OH