题目内容
T℃时,A、B、C三种气体在反应过程中的浓度变化如图1所示,若保持其它条件不变,温度分别为T1℃和T2℃时,B的浓度变化与时间的关系示意图如图2所示.

请回答下列问题:
(1)该反应的化学反应方程式是:
(2)比较大小:
A和B的转化率A B,原因是 ;
温度的高低T1 T2,判断依据是 .
(3)若其它条件不变,反应进行到(t1+10)min时,A的浓度为 .

请回答下列问题:
(1)该反应的化学反应方程式是:
(2)比较大小:
A和B的转化率A
温度的高低T1
(3)若其它条件不变,反应进行到(t1+10)min时,A的浓度为
考点:化学平衡的计算,化学平衡的影响因素
专题:化学平衡专题
分析:(1)随反应进行,A、B的物质的量浓度减小,为反应物,C的物质的量浓度增大,为生成物,最终A、B的浓度不变化,且不为0,属于可逆反应,利用浓度变化量之比等于化学计量数之比确定化学计量数,据此书写;
(2)根据起始浓度之比与化学计量数之比判断;达到平衡的时间越短,反应速率越快,温度越高;
(3)t1时刻,到达平衡状态,各组分的浓度不再变化.
(2)根据起始浓度之比与化学计量数之比判断;达到平衡的时间越短,反应速率越快,温度越高;
(3)t1时刻,到达平衡状态,各组分的浓度不再变化.
解答:
解:(1)随反应进行,A、B的物质的量浓度减小,为反应物,C的物质的量浓度增大,为生成物,最终A、B的浓度不变化,且不为0,属于可逆反应,A、B、C的化学计量数之比=(0.5-0.3):(0.7-01):0.4=1:3:2,故反应方程式为:A(g)+3B(g)?2C(g),故答案为:A(g)+3B(g)?2C(g);
(2)A、B的起始浓度之比等于化学计量数之比,二者转化率相等,加入的A、B浓度比=5:7=1:1.4,大于参加反应的A、B浓度比1:3,故转化率A<B;
从图2判断,T1时,达到平衡的时间短,说明反应速率快,所以温度高,故温度T1>T2,
故答案为:<,加入的A、B浓度比=5:7=1:1.4,大于参加反应的A、B浓度比1:3;>,从图2判断,T1时,达到平衡的时间短,说明反应速率快,所以温度高;
(3)t1时刻,到达平衡状态,各组分的浓度不再变化,故反应进行到(t1+10)min时,A的浓度为0.3mol?L-1,故答案为:0.3mol?L-1.
(2)A、B的起始浓度之比等于化学计量数之比,二者转化率相等,加入的A、B浓度比=5:7=1:1.4,大于参加反应的A、B浓度比1:3,故转化率A<B;
从图2判断,T1时,达到平衡的时间短,说明反应速率快,所以温度高,故温度T1>T2,
故答案为:<,加入的A、B浓度比=5:7=1:1.4,大于参加反应的A、B浓度比1:3;>,从图2判断,T1时,达到平衡的时间短,说明反应速率快,所以温度高;
(3)t1时刻,到达平衡状态,各组分的浓度不再变化,故反应进行到(t1+10)min时,A的浓度为0.3mol?L-1,故答案为:0.3mol?L-1.
点评:本题考查化学平衡图象、化学平衡计算与影响因素,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
目前,全世界提倡“低碳生活”的理念,号召大家减少使用能产生CO2的燃料.下列燃料燃烧时不会产生CO2的是( )
| A、煤 | B、天然气 | C、石油 | D、氢气 |
为实现“绿色奥运”,下列建议不合理的是( )
| A、推广使用无磷洗涤剂 |
| B、推广垃圾分类存放、回收和处理 |
| C、提倡使用手帕,减少餐巾纸的使用 |
| D、提倡使用一次性塑料餐具和塑料袋 |
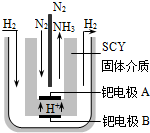 现在普遍应用的工业合成氨的方法是哈伯于1905年发明的,但此法反应物的转化率不高.
现在普遍应用的工业合成氨的方法是哈伯于1905年发明的,但此法反应物的转化率不高.

 2012年3月,新《环境空气质量标准》的颁布表明国家对环境问题的进一步重视.
2012年3月,新《环境空气质量标准》的颁布表明国家对环境问题的进一步重视. 已知A是应用最广泛、用量最大的一种金属单质,B是黑色固体,C是气体单质,在一定条件下有下列转化关系:
已知A是应用最广泛、用量最大的一种金属单质,B是黑色固体,C是气体单质,在一定条件下有下列转化关系: