题目内容
(12分)利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下: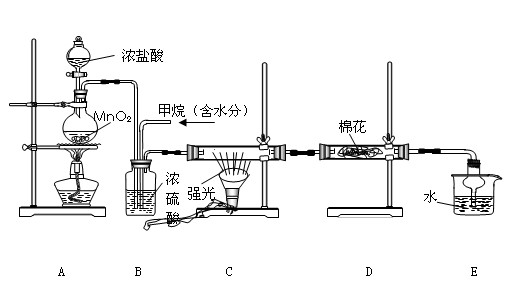
(1)写出A装置中发生反应的离子方程式
(2)B装置有三种功能:①控制气流速度;②均匀混合气体;③
(3)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应≥
(4)一段时间后发现D装置中的棉花由白色变为蓝色,则棉花上可能预先滴![]() 有 溶液。
有 溶液。
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出反应的化学方程式 。
(6) E装置中除盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为 (填字母)。
![]() A.水洗分液法 B.蒸馏法 C.萃取分液法 D.结晶法
A.水洗分液法 B.蒸馏法 C.萃取分液法 D.结晶法
(7) 该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为 (填字母)。
![]() A、CH4 B、CH3Cl C、CH2Cl2 D、CHCl3
A、CH4 B、CH3Cl C、CH2Cl2 D、CHCl3
(1)MnO2+4H+ +2Cl -(浓)=Mn2+ +Cl2↑+2H2O (2分)
(2)干燥气体(1分)
(3)4 (2分)
(4)KI淀粉溶液(1分)
(5)CH4+2Cl2 → C+4HCl (2分)
(6) A (2分)
(7)AB (2分)

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案(15分)工来合成氨与制备硝酸一般可连续生产,流程如下:
(1)工来生产时,制取氢气的一个反应为:![]() ,
,
①t℃时,往l L密闭容器中充人0.2 mol CO和0.3 mol水蒸气,反应建立平衡后,体系中c(H2)=0.12 mol?L-1,该温度下此反应的平衡常数K= ;
②保持温度不变,向上述平衡体系中再加入0.1 mol CO,当反应重新建立平衡时,水蒸气的总转化率![]() (H2O)= 。
(H2O)= 。
T(K) | T1 | 573 | T2 |
K | 1.00×107 | 2.45×105 | 1.88×103 |
(2)合成塔中发生反应为:
![]()
![]()
 右表为不同温度下该反应的平衡常数。由此可推知,表中T1 573K(填“>”、“<”或“=”)。
右表为不同温度下该反应的平衡常数。由此可推知,表中T1 573K(填“>”、“<”或“=”)。
(3)NH3和O2在铂系催化剂作用下从145℃就开始反应:
![]() 4NH3+5O2
4NH3+5O2![]() NO+6H2O AH=-905kJ?mol-1,不同温度下NO产率如图所示,温度高于900℃时,NO产率下降的原因 。
NO+6H2O AH=-905kJ?mol-1,不同温度下NO产率如图所示,温度高于900℃时,NO产率下降的原因 。
![]() (4)吸收塔中反应为:3NO2+H2O
(4)吸收塔中反应为:3NO2+H2O![]() 2HNO3+NO。从生产流程看,吸收塔中需要补充空气,其原因是
2HNO3+NO。从生产流程看,吸收塔中需要补充空气,其原因是
![]() (5)硝酸厂的尾气含有氮氧化物,不经处理直接排放将污染空气。目前科学家探索利用燃料气体中的甲烷将氮氧化物还原为氮气和水,其反应机理为:
(5)硝酸厂的尾气含有氮氧化物,不经处理直接排放将污染空气。目前科学家探索利用燃料气体中的甲烷将氮氧化物还原为氮气和水,其反应机理为:
![]() CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ![]() H=-574kJ?mol-1。;
H=-574kJ?mol-1。;
![]() CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ![]() H=-1160 kJ?mol-1;
H=-1160 kJ?mol-1;
则甲烷直接将NO2还原为N2的热化学方程式为: 。
