题目内容
14.汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2+Pb+2H2SO4═2PbSO4+2H2O,根据此反应判断下列叙述中正确的是( )| A. | PbO2是电池的负极 | |
| B. | PbO2得电子,被氧化 | |
| C. | 电池放电时,溶液酸性增强 | |
| D. | 负极的电极反应式为:Pb+SO42--2e -═PbSO4 |
分析 放电时,该装置是原电池,负极上失电子发生氧化反应,正极上得电子发生还原反应,据此分析解答.
解答 解:A.根据电池反应式知,二氧化铅得电子发生还原反应,所以二氧化铅是正极,故A错误;
B.二氧化铅得电子被还原,故B错误;
C.电池放电时,硫酸参加反应生成水,所以溶质的质量减少,溶剂的质量增加,所以溶液酸性减弱,故C错误;
D.负极上铅失电子和硫酸根离子反应生成硫酸铅,电极反应式为:Pb(s)+SO42-(aq)-2e-=PbSO4(s),故D正确;
故选D.
点评 本题考查了二次电池的有关知识,难度不大,注意根据反应方程式判断电解池和原电池,特别是电极反应式的书写,学习中注意体会书写方法.

练习册系列答案
相关题目
1.下列叙述中,正确的是( )
| A. | 11.2LH2中含有的氢原子一定为1mol | |
| B. | 16gCH4在标准状况下的体积约为22.4L | |
| C. | 71gCl2中含有的氯原子数约为6.02×1023 | |
| D. | 1L 0.5 mol/LBaCl2溶液中Cl-的物质的量浓度为0.5 mol/L |
5.用分液漏斗可以分离的一组混合物是( )
| A. | 氯化钠和水 | B. | 苯和水 | C. | 水和酒精 | D. | 泥沙和水 |
9.乙醇在发生催化氧化时,化学键断裂的位置是(如图)( )


| A. | ②③ | B. | ③④ | C. | ①③ | D. | ②④ |
3.长途运输中,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛有水果的容器中,其原因是( )
| A. | 利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变 | |
| B. | 利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂 | |
| C. | 利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟 | |
| D. | 利用高锰酸钾溶液的氧化性,催熟水果 |
4.下列物质属于非电解质的是( )
| A. | 稀硫酸 | B. | Cu | C. | SO2 | D. | NaOH |
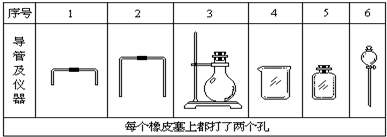
 科学家致力于二氧化碳的“组合转化”技术的研究,把过多二氧化碳转化为有益于人类的物质.
科学家致力于二氧化碳的“组合转化”技术的研究,把过多二氧化碳转化为有益于人类的物质. 代表氢原子,
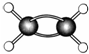
代表氢原子, 代表碳原子)和水,该有机物的结构简式为CH2=CH2.
代表碳原子)和水,该有机物的结构简式为CH2=CH2.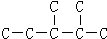 ,该烷烃的名称为2,3-二甲基戊烷;其一溴代物有6种.
,该烷烃的名称为2,3-二甲基戊烷;其一溴代物有6种.