题目内容
常温时,将等质量的AgCl固体分别加入到等体积的下列4种溶液中,AgCl溶解最少的是( )
| A、1mol/L的AlCl3溶液 |
| B、2mol/L的NaCl溶液 |
| C、1.4mol/L的BaCl2溶液 |
| D、1mol/L的MgCl2溶液 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:依据氯化银在水溶液中存在沉淀溶解平衡,AgCl(s)?Ag++Cl-;结合选项中 氯离子浓度大小影响平衡移动方向分析氯化银的溶解度大小.
解答:
解:A、氯离子浓度3mol/L;
B、氯离子浓度2mol/L;
C、氯离子浓度2.8mol/L;
D、氯离子浓度2mol/L;
所以氯离子浓度越大对沉淀溶解平衡抑制程度越大,氯化银溶解度越小,故D选项氯离子浓度最大,氯化银溶解度最小;
故选A.
B、氯离子浓度2mol/L;
C、氯离子浓度2.8mol/L;
D、氯离子浓度2mol/L;
所以氯离子浓度越大对沉淀溶解平衡抑制程度越大,氯化银溶解度越小,故D选项氯离子浓度最大,氯化银溶解度最小;
故选A.
点评:本题考查沉淀溶解平衡的影响因素分析判断,主要是氯离子浓度大小对平衡的影响判断,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列过程溶液可能会变浑浊的有( )
①钠投入饱和食盐水中;
②少量钠投入饱和NaHCO3溶液中;
③过量的CO2通入饱和Na2CO3溶液中;
④过量的CO2通入CaCl2溶液中;
⑤足量的BaCl2溶液加入NaHCO3溶液中.
①钠投入饱和食盐水中;
②少量钠投入饱和NaHCO3溶液中;
③过量的CO2通入饱和Na2CO3溶液中;
④过量的CO2通入CaCl2溶液中;
⑤足量的BaCl2溶液加入NaHCO3溶液中.
| A、①② | B、①③ |
| C、①③④⑤ | D、①②③④⑤ |
 历史上最早应用的还原性染料是靛蓝,其结构简式如图.下列关于靛蓝的叙述中错误的是( )
历史上最早应用的还原性染料是靛蓝,其结构简式如图.下列关于靛蓝的叙述中错误的是( )| A、靛蓝由碳、氢、氧、氮四种元素组成 |
| B、它的分子式是C16H10N2O2 |
| C、该物质苯环上的一溴代物有两种 |
| D、1mol靛蓝最多可与9mol氢气加成 |
在标准状况下,相同质量的下列气体中体积最大的是( )
| A、H2O |
| B、Cl2 |
| C、N2 |
| D、CO2 |
将足量的AgCl固体分别放入下列体系中,充分溶解至溶液饱和,其中c(Ag+)最大的是( )
| A、5mL水 |
| B、10 mL 0.2 mol?L-1 MgCl2溶液 |
| C、20 mL 0.5 mol?L-1 NaCl溶液 |
| D、40mL 0.1 mo1?L-1盐酸 |
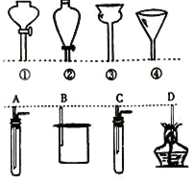 ①②③④分别是几种常用漏斗的上部,A、B、C、D是实际应用操作(分液、制气、向容器中加液体试剂等)时,各种漏斗的下部插入容器中的示意图(仪器中的药品及铁架台、铁夹等其它物品均已略去).请根据实际使用操作时上述漏斗的适用范围和它们的形状,指出A、B、C、D分别与①②③④中哪一种或哪几种最为匹配.A与
①②③④分别是几种常用漏斗的上部,A、B、C、D是实际应用操作(分液、制气、向容器中加液体试剂等)时,各种漏斗的下部插入容器中的示意图(仪器中的药品及铁架台、铁夹等其它物品均已略去).请根据实际使用操作时上述漏斗的适用范围和它们的形状,指出A、B、C、D分别与①②③④中哪一种或哪几种最为匹配.A与