题目内容
1.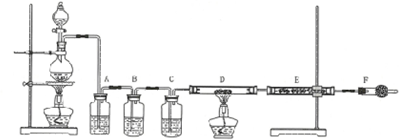 过量的锌与浓硫酸作用的全过程中产生的气体可能有多种.有人认为气体中可能有SO2,也可能有H2.为了说明这两种气体的有无,设计了如图所示的实验装置.
过量的锌与浓硫酸作用的全过程中产生的气体可能有多种.有人认为气体中可能有SO2,也可能有H2.为了说明这两种气体的有无,设计了如图所示的实验装置.(1)将仪器安装连接好之后,必须进行的一步操作是检验装置的气密性.
(2)在实验中要用到的试剂有:a.浓硫酸,b.锌,c.无水硫酸铜,d.氧化铜,e.品红溶液,f.KMnO4溶液,g.碱石灰.
将试剂的序号字母填入有关仪器的空白中,应盛入的试剂:
A中e,B中f,C中a,
D中d,E中c,F中g.
(3)说明气体中有SO2,在仪器(填编号字母,下同)A中的现象是品红溶液颜色褪去.
(4)说明试验中出来的气体中有氢气,主要应在实验开始时,还是反应后期时?反应后期;在装置DE中的现象是D装置中观察到黑色固体变红,E中白色固体变蓝色;产生氢气的可能原因是随着反应的进行硫酸变稀,与锌反应生成氢气.
(5)仪器C中放入试剂的作用是干燥进入CuO的氢气.若不放它,会导致不能说明使无水硫酸铜变蓝的水是氢气还原氧化铜而来,且损坏硬质玻璃管E.
(6)仪器F的作用是防止空气中的水蒸气进入E中.
分析 浓硫酸具有强氧化性,金属锌具有还原性,Zn与浓H2SO4反应生成硫酸锌、二氧化硫和水,反应的方程式为:Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4+SO2↑+2H2O,随反应进行,浓硫酸变为稀硫酸,Zn与稀硫酸反应生成硫酸锌与氢气.装置A的作用为检验气体X中有二氧化硫,通常使用品红溶液;酸性高锰酸钾溶液除去二氧化硫,B装置吸收水蒸气,C用于干燥气体,D中氢气与CuO发生置换反应,E中硫酸铜吸水,根据D固体颜色变化或E中硫酸铜颜色变化,判断是否有氢气生成,F中可以盛放碱石灰,防止空气中水蒸气加入E中,以此解答该题.
解答 解:浓硫酸具有强氧化性,金属锌具有还原性,Zn与浓H2SO4反应生成硫酸锌、二氧化硫和水,反应的方程式为:Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4+SO2↑+2H2O,随反应进行,浓硫酸变为稀硫酸,Zn与稀硫酸反应生成硫酸锌与氢气.装置A的作用为检验气体X中有二氧化硫,通常使用品红溶液;酸性高锰酸钾溶液除去二氧化硫,B装置吸收水蒸气,C用于干燥气体,D中氢气与CuO发生置换反应,E中硫酸铜吸水,根据D固体颜色变化或E中硫酸铜颜色变化,判断是否有氢气生成,F中可以盛放碱石灰,防止空气中水蒸气加入E中,
(1)因反应有气体生成,实验时应先检查气密性,防止实验失败,故答案为:检验装置的气密性;
(2)由以上分析可知A中药品为品红溶液,B中药品为KMnO4溶液,C中药品为浓硫酸,D中药品为氧化铜,E中药品为无水硫酸铜,F中药品为碱石灰,
故答案为:e;f;a;d;c;g;
(3)如由二氧化硫生成,则A中品红溶液颜色褪去,故答案为:A;品红溶液颜色褪去;
(4)开始时硫酸浓度较大,与锌反应生成二氧化硫气体,随着反应的进行,硫酸浓度减小,则到后期时生成氢气,可在D装置中观察到黑色固体变红,E中白色固体变蓝色,
故答案为:反应后期;DE;D装置中观察到黑色固体变红,E中白色固体变蓝色;随着反应的进行硫酸变稀,与锌反应生成氢气;
(5)仪器C中放入试剂为浓硫酸,作用是干燥进入CuO的氢气,否则不能说明使无水硫酸铜变蓝的水是氢气还原氧化铜而来,且损坏硬质玻璃管E,
故答案为:干燥进入CuO的氢气;干燥进入CuO的氢气,否则不能说明使无水硫酸铜变蓝的水是氢气还原氧化铜而来,且损坏硬质玻璃管E;
(6)碱石灰的主要成分为氧化钙和氢氧化钠,能吸收水和二氧化碳,为防止空气中的水蒸气进入E中而干扰实验现象,
故答案为:防止空气中的水蒸气进入E中.
点评 本题考查锌和硫酸的反应及产物的检验,题目难度中等,注意掌握浓硫酸的性质,根据需检验气体的性质、检验方法理解检验的先后顺序是解答的关键.

| A. | 纯碱和熟石灰都是碱 | |
| B. | 粗盐和酸雨都是混合物 | |
| C. | 盐酸和食醋既是化合物又是酸 | |
| D. | 生石灰与水混合的过程只发生物理变化 |
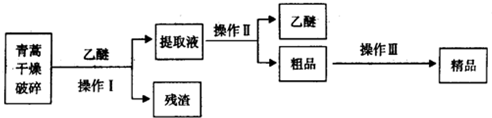
(1)对青蒿进行干燥破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率;
(2)操作I需要的玻璃仪器主要有:烧杯、漏斗、玻璃棒,操作Ⅱ的名称是蒸馏;
(3)操作Ⅲ的主要过程可能是B(填字母);
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算.
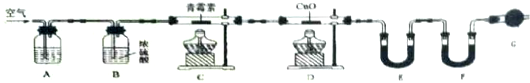
①装置A、E、F中盛放的物质分别是NaOH溶液、CaCl2或P2O5、碱石灰;
②G的作用是防止空气中的CO₂和水蒸气进入F的装置;
③
| 装置 | 实验前/g | 实验后/g |
| E | 22.6 | 42.4 |
| F | 80.2 | 146.2 |
(5)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与C(填字母)具有相同的性质;
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
(6)某科研小组经多次提取青蒿素实验认为用石油醚做溶剂较为适宜,实验中通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如图所示:
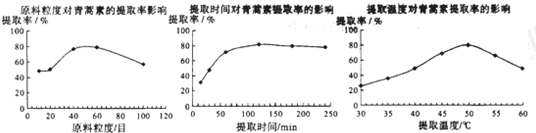
由上图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为B.
A.80目、100分钟、50℃B.60目、120分钟、50℃C.60目、120分钟、55℃
| A. | 并不是所有物质都含有化学键 | B. | 只有非金属原子间才能形成共价键 | ||
| C. | 单质不可能含有离子键 | D. | 共价化合物中不可能含有离子键 |
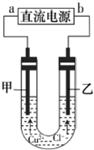
| A. | b端是直流电源的负极 | |
| B. | 用湿润的KI一淀粉试纸检验甲电极产物 | |
| C. | 通电一段时间后,在阴极附近观察到黄绿色气体 | |
| D. | 若将甲电极换成铁棒,乙电极换成铜棒,则可实现在铁棒上镀铜 |
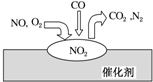 在汽车尾气净化装置里,气体在催化剂表面吸附与释放的过程如图所示.下列说法正确的是( )
在汽车尾气净化装置里,气体在催化剂表面吸附与释放的过程如图所示.下列说法正确的是( )| A. | NO是该过程的中间产物 | |
| B. | NO和O2必须在催化剂表面才能反应 | |
| C. | 汽车尾气的主要污染成分包括CO2和NO | |
| D. | 汽车尾气的主要污染物是CO和NO |
| A. | N5+离子中含有36个电子 | B. | O2与O4属于同位素 | ||
| C. | C60比金刚石熔点高 | D. | H2与H3属于同素异形体 |
 根据下列图示变化及已知条件填空.
根据下列图示变化及已知条件填空.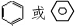 .乙烯与溴水的反应是加成反应.把甲烷和氯气混合在一起的试管倒置在装有饱和食盐水的水槽中进行光照有几种产物5种,最多的是氯化氢.
.乙烯与溴水的反应是加成反应.把甲烷和氯气混合在一起的试管倒置在装有饱和食盐水的水槽中进行光照有几种产物5种,最多的是氯化氢.