��Ŀ����
9����֪���з�Ӧ������Ӧ������������������ʵĻ�ѧ������������ȥ������A+B $\stackrel{���}{��}$ M+D+E�� ��M+E��A+F+B
������������ֲ�ͬ����ش�
��1����A��һ�����Σ���Ӧ���ǻ�ѧ��ҵ����ȡ����E�ͻ�����M����Ҫ��������A�ĵ���ʽΪ
 ��
����Ӧ�ڵ����ӷ���ʽΪCl2+2OH-�TCl-+ClO-+H2O��
�����������£�����������F�ӵ�Fe2+����Һ�У���Һ��dz��ɫ��ɻ�ɫ����Ӧ�����ӷ���ʽΪ2Fe2++ClO-+2H+�T2Fe3++Cl-+H2O��
��2����A��һ�ֺ������Σ�������ʵ�����м���ˮ�Ĵ��ڣ�1��A����������й�����50�����ӣ����к���һ��Ԫ��X��X��ԭ�ӵ������������ǵ��Ӳ�����2������X��Ԫ�����ڱ��е�λ����������VIA�壮X���ʵ��۵���112.8�棬��X���ʵľ����������ڷ��Ӿ��壮
X��̼������һ�������¿�������CX2�Ļ��������ӽṹ������CO2����CX2���ڷǼ��Է��ӣ�����ԡ��Ǽ��ԡ�������Ӧ�ڵĻ�ѧ����ʽΪ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
���� ��1��A��һ�����Σ���Ӧ���ǻ�ѧ��ҵ����ȡ����E�ͻ�����M����Ҫ�����������������£�����������F�ӵ�Fe2+����Һ�У���Һ��dz��ɫ��ɻ�ɫ��F����ǿ�����ԣ���Ӧ�ǵ�ⱥ��ʳ��ˮ�ķ�Ӧ��AΪNaCl��BΪH2O��MΪNaOH��EΪCl2��DΪH2��FΪNaClO��
��2����A��һ�ֺ������Σ�������ʵ�����м���ˮ�Ĵ��ڣ�1��A����������й�����50�����ӣ����к���һ��Ԫ��X��X��ԭ�ӵ������������ǵ��Ӳ�����2����XΪSԪ�ء����ΪSO42-��AΪCuSO4��BΪH2O����Ӧ��ӦΪŨ�����Cu�ķ�Ӧ����֪EΪCu��MΪH2SO4��AΪCuSO4����Ӧ��Ӧ�ڵ�������½��У�DӦΪO2��
��� �⣺��1��A��һ�����Σ���Ӧ���ǻ�ѧ��ҵ����ȡ����E�ͻ�����M����Ҫ�����������������£�����������F�ӵ�Fe2+����Һ�У���Һ��dz��ɫ��ɻ�ɫ��F����ǿ�����ԣ���Ӧ�ǵ�ⱥ��ʳ��ˮ�ķ�Ӧ��AΪNaCl��BΪH2O��MΪNaOH��EΪCl2��DΪH2��FΪNaClO����A�ĵ���ʽΪ ����Ӧ�ڵ����ӷ���ʽΪCl2+2OH-�TCl-+ClO-+H2O��
����Ӧ�ڵ����ӷ���ʽΪCl2+2OH-�TCl-+ClO-+H2O��
�����������£�����������F�ӵ�Fe2+����Һ�У���Һ��dz��ɫ��ɻ�ɫ����Ӧ�����ӷ���ʽΪ��2Fe2++ClO-+2H+�T2Fe3++Cl-+H2O��
�ʴ�Ϊ�� ��Cl2+2OH-�TCl-+ClO-+H2O��2Fe2++ClO-+2H+�T2Fe3++Cl-+H2O��
��Cl2+2OH-�TCl-+ClO-+H2O��2Fe2++ClO-+2H+�T2Fe3++Cl-+H2O��
��2����A��һ�ֺ������Σ�������ʵ�����м���ˮ�Ĵ��ڣ�1��A����������й�����50�����ӣ����к���һ��Ԫ��X��X��ԭ�ӵ������������ǵ��Ӳ�����2����XΪSԪ�ء����ΪSO42-��AΪCuSO4��BΪH2O����Ӧ��ӦΪŨ�����Cu�ķ�Ӧ����֪EΪCu��MΪH2SO4��AΪCuSO4����Ӧ��Ӧ�ڵ�������½��У�DӦΪO2����X��Ԫ�����ڱ��е�λ���ǵ�������VIA�壮���ʵ��۵���112.8�棬�����ʵľ������ڷ��Ӿ��壻
X��̼������һ�������¿�������CS2�Ļ��������ӽṹ������CO2��Ϊֱ���ͶԳƽṹ����CS2���ڷǼ��Է��ӣ���Ӧ�ڵĻ�ѧ����ʽΪ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
�ʴ�Ϊ������VIA�����ӣ��Ǽ��ԣ�Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
���� ���⿼��������ƶϣ�������ѧ���ķ��������ͼ��������Ŀ��飬ע���������յ���ԭ�����ɣ���Ϸ�Ӧ���ص��Լ���������ƶϣ��Ѷ��еȣ�

 ���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д�
���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д� ���Ͱ�ͨ������ϵ�д�
���Ͱ�ͨ������ϵ�д� �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д�| A�� | ��ˮ�������c��H+��=1��10-13mol/L����Һ����������һ���ܴ������棺Na+��CO32-��Cl-��K+ | |
| B�� | ����������Ũ����ͬ������������Һ�Ͱ�ˮ����������ͬ | |
| C�� | K2SO3��Һ��c��K+����c��SO32-��֮��Ϊ2��1 | |
| D�� | ������ǿ����ʣ��ʴ������ܵ��� |
| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO��/mol | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
��2����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����AD
A��������ѹǿ���� B��������������ܶȱ��ֲ���
C��v����NO��=2v����O2�� D��v����NO2��=v����NO2��
 �£�N2H4�������������ڰ�����������ˮ�������ϡ����ݼ���ԭ�ϣ���������ͨ��Cu0�����У��ɷ�����ͼ��ʾ��ת����
�£�N2H4�������������ڰ�����������ˮ�������ϡ����ݼ���ԭ�ϣ���������ͨ��Cu0�����У��ɷ�����ͼ��ʾ��ת���� ������ͭ��Cu2O����Ϊһ����Ҫ��������ԭ�ϣ������ϡ���ɫ�����ʹ������������Ź㷺����;���ش��������⣺
������ͭ��Cu2O����Ϊһ����Ҫ��������ԭ�ϣ������ϡ���ɫ�����ʹ������������Ź㷺����;���ش��������⣺ Ԫ�ؼ��仯�������������������й㷺Ӧ�ã���ش��������⣺
Ԫ�ؼ��仯�������������������й㷺Ӧ�ã���ش��������⣺ ��
�� ��
��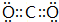 ��
�� ��
�� �������������������CO����Ⱦ��Ҳ�ɶ����ⶨCO�������䷴Ӧԭ��Ϊ
�������������������CO����Ⱦ��Ҳ�ɶ����ⶨCO�������䷴Ӧԭ��Ϊ