题目内容
11.参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
| A. | 正反应为放热反应 | |
| B. | 加入催化剂,该化学反应的反应热不变 | |
| C. | 反应物总能量高于生成物总能量 | |
| D. | 升高温度可增大正反应速率,降低逆反应速率 |
分析 根据反应物的总能量小于生成物的总能量,可知反应吸热,
A、正反应为吸热反应;
B、催化剂与反应热无关;
C、正反应为吸热反应;
D、升高温度可增大正反应速率,也增大逆反应速率.
解答 解:根据反应物的总能量小于生成物的总能量,可知反应吸热,
A、反应物的总能量小于生成物的总能量,则正反应为吸热反应,故A错误;
B、催化剂只能降低反应所需的活化能,与反应热大小无关,故B正确;
C、正反应为吸热反应,反应物总能量低于生成物总能量,故C错误;
D、升高温度,活化分子百分数增大,有效碰撞几率增大,反应速率增大,则可增大正反应速率,也增大逆反应速率,故D错误;
故选B.
点评 本题考查反应热,要掌握反应物的总能量小于生成物的总能量,反应吸热,反应物的总能量大于生成物的总能量,反应放热,题目难度不大.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案
相关题目
1.下列物质暴露在空气中不易变质的是( )
| A. | 氯化钠 | B. | 氢氧化钠 | C. | 溴化银 | D. | 漂白粉 |
19.在一定条件下,反应CO+NO2?CO2+NO△H=a kJ/mol达到平衡后,降低温度,混和气体的颜色变浅.下列判断正确的是( )
| A. | a<0 | |
| B. | 降低温度,各物质的浓度不变 | |
| C. | 降低温度,CO的平衡转化率降低 | |
| D. | 使用催化剂能加快反应速率并提高反应物的平衡转化率 |
16.下列说法不正确的是( )
| A. | ${\;}_{\;}^{12}$C和${\;}_{\;}^{14}$C互为同位素 | |
| B. | 乙醇与二甲醚(CH3-O-CH3)互为同分异构体 | |
| C. | 红磷与白磷互为同素异形体 | |
| D. | H2O与D2O互为同位素 |
5.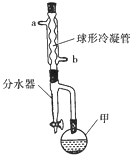 乙酸异戊酯常作为配制香蕉、梨、苹果等多种口味食品的香料.实验室合成乙酸异戊酯的原料是乙酸和异戊醇[(CH3)2CHCH2CH2OH],其装置如图所示.
乙酸异戊酯常作为配制香蕉、梨、苹果等多种口味食品的香料.实验室合成乙酸异戊酯的原料是乙酸和异戊醇[(CH3)2CHCH2CH2OH],其装置如图所示.
合成反应:
在甲中加入20g异戊醇和少量碎瓷片,在不断搅拌下加入2mL浓硫酸,冷却后加入100g稍过量的冰醋酸,再加入环己烷(能与产物形成共沸混合物,不参加反应).安装带有分水器(预装有一定量的水)的冷凝回流装置,球形冷凝管中通入冷却水,用甘油浴缓慢加热仪器甲,冷凝回流一段时间.
分离提纯:
将反应粗产品倒入分液漏斗中,分别用少量10% Na2CO3溶液分两次洗涤.分去水层,向有机层中加入无水硫酸镁固体,静置一段时间后分离出液体,最后蒸馏除去环己烷得到纯净的乙酸异戊酯13g.
已知下列物质的沸点和密度:
请回答下列问题:
(1)合成乙酸异戊酯的化学方程式为CH3COOH+(CH3)2CHCH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH(CH3)2+H2O.
(2)仪器甲的名称是圆底烧瓶.
(3)分水器可将仪器甲中产生的水分离出来,目的是提高反应物的转化率或生成物的产率;按照球形冷凝管中冷却水的流向应该由b(填“a”或“b”)口进水.
(4)本实验使用甘油浴加热的优点有便于控制反应温度、使圆底烧瓶受热均匀 (答出两点即可).
(5)当观察到分水器中出现水层高度(或水的体积、液面对应刻度)不再变化现象时,可停止加热仪器甲,终止合成反应过程.
(6)用10%Na2CO3溶液洗涤的作用是ad.
a、除去未反应完的醋酸 b、提高异戊醇的转化率
c、与异戊醇反应,除去杂质 d、降低乙酸异戊酯在水中的溶解能力
(7)本实验中无水硫酸镁的作用是作干燥剂.
(8)本实验中异戊醇的转化率为44%.
 乙酸异戊酯常作为配制香蕉、梨、苹果等多种口味食品的香料.实验室合成乙酸异戊酯的原料是乙酸和异戊醇[(CH3)2CHCH2CH2OH],其装置如图所示.
乙酸异戊酯常作为配制香蕉、梨、苹果等多种口味食品的香料.实验室合成乙酸异戊酯的原料是乙酸和异戊醇[(CH3)2CHCH2CH2OH],其装置如图所示.合成反应:
在甲中加入20g异戊醇和少量碎瓷片,在不断搅拌下加入2mL浓硫酸,冷却后加入100g稍过量的冰醋酸,再加入环己烷(能与产物形成共沸混合物,不参加反应).安装带有分水器(预装有一定量的水)的冷凝回流装置,球形冷凝管中通入冷却水,用甘油浴缓慢加热仪器甲,冷凝回流一段时间.
分离提纯:
将反应粗产品倒入分液漏斗中,分别用少量10% Na2CO3溶液分两次洗涤.分去水层,向有机层中加入无水硫酸镁固体,静置一段时间后分离出液体,最后蒸馏除去环己烷得到纯净的乙酸异戊酯13g.
已知下列物质的沸点和密度:
| 甘油 | 环已烷 | 乙酸 | 异戊醇 | |
| 沸点/℃ | 290 | 80.7 | 117.9 | 132.5 |
| 密度/g•cm-3 | 1.26 | 0.78 | 1.05 | 0.81 |
(1)合成乙酸异戊酯的化学方程式为CH3COOH+(CH3)2CHCH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH(CH3)2+H2O.
(2)仪器甲的名称是圆底烧瓶.
(3)分水器可将仪器甲中产生的水分离出来,目的是提高反应物的转化率或生成物的产率;按照球形冷凝管中冷却水的流向应该由b(填“a”或“b”)口进水.
(4)本实验使用甘油浴加热的优点有便于控制反应温度、使圆底烧瓶受热均匀 (答出两点即可).
(5)当观察到分水器中出现水层高度(或水的体积、液面对应刻度)不再变化现象时,可停止加热仪器甲,终止合成反应过程.
(6)用10%Na2CO3溶液洗涤的作用是ad.
a、除去未反应完的醋酸 b、提高异戊醇的转化率
c、与异戊醇反应,除去杂质 d、降低乙酸异戊酯在水中的溶解能力
(7)本实验中无水硫酸镁的作用是作干燥剂.
(8)本实验中异戊醇的转化率为44%.
2.制备硅单质时,化学反应如下:(1)SiO2+2C═Si+2CO↑ (2)Si+2Cl2═SiCl4 (3)SiCl4+2H2═Si+4HCl.下列对上述三个反应的叙述中,不正确的是( )
| A. | (1)(3)为置换反应 | |
| B. | (1)(2)(3)均为氧化还原反应 | |
| C. | (2)为化合反应 | |
| D. | 三个反应的反应物中硅元素均被还原 |
3.下列选项中最后的物质是要制取的物质,其中不可能得到的是( )
| A. | CaCO3$\stackrel{高温}{→}$CaO$\stackrel{H_{2}O}{→}$Ca(OH)2$→_{过滤}^{Na_{2}CO_{3}}$NaOH溶液 | |
| B. | Cu$→_{△}^{O_{2}}$CuO$→_{△}^{H_{2}SO_{4}}$CuSO4溶液$→_{过滤}^{NaOH溶液}$Cu(OH)2沉淀 | |
| C. | KMnO4$\stackrel{△}{→}$O2$\stackrel{点燃S}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4溶液 | |
| D. | BaCO3$\stackrel{盐酸}{→}$BaCl2溶液$\stackrel{通入H_{2}SO_{4}}{→}$BaSO4沉淀 |