题目内容
下列实验操作正确的是( )
A、 称量氢氧化钠固体 |
B、 配制150mL0.10mol/L盐酸 |
C、 检验铁粉与水蒸气反应产生的氢气 |
D、 分离两种互溶但沸点相差较大的液体混合物 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.称量时,左物右码,且NaOH应在小烧杯中称量;
B.容量瓶选择错误;
C.Fe与水蒸气反应生成四氧化三铁和氢气,点燃肥皂泡验证氢气;
D.冷水水方向错误.
B.容量瓶选择错误;
C.Fe与水蒸气反应生成四氧化三铁和氢气,点燃肥皂泡验证氢气;
D.冷水水方向错误.
解答:
解:A.称量操持不合理,物体应在左盘,且NaOH易潮解应在小烧杯中称量,故A错误;
B.配制150mL 0.10 mol?L-1盐酸,应选择150mL容量瓶,故B错误;
C.Fe与水蒸气反应生成四氧化三铁和氢气,点燃肥皂泡验证氢气,图中实验装置及方案合理,故C正确;
D.蒸馏实验中,冷却水应下进上出,图中冷却水方向不合理,故D错误;
故选C.
B.配制150mL 0.10 mol?L-1盐酸,应选择150mL容量瓶,故B错误;
C.Fe与水蒸气反应生成四氧化三铁和氢气,点燃肥皂泡验证氢气,图中实验装置及方案合理,故C正确;
D.蒸馏实验中,冷却水应下进上出,图中冷却水方向不合理,故D错误;
故选C.
点评:本题考查化学实验方案的评价,为高频考点,涉及固体称量、溶液配制、金属的性质、分馏等,把握实验操作的规范性、实验细节和实验原理为解答的关键,注意方案的合理性、评价性、操作性分析,选项C为解答的难点,题目难度不大.

练习册系列答案
相关题目
工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图.下列说法不正确的是( )
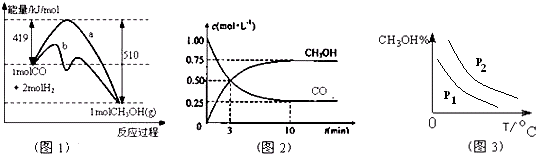

| A、曲线b表示使用了催化剂;该反应属于放热反应 |
| B、当压强不同时(P1<P2)时,平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线如图3 |
| C、容器中压强恒定时,反应已达平衡状态 |
| D、该温度下CO(g)+2H2(g)?CH3OH(g)的化学平衡常数为10 |
下列判断或叙述正确的是( )
| A、某无色溶液中加入AgNO3溶液得白色沉淀,加稀硝酸沉淀不消失,则原液一定存在Cl- |
| B、某无色溶液中滴加BaCl2溶液得白色沉淀,加稀硝酸沉淀不溶解,则一定含有SO42- |
| C、提纯含有少量Ba(NO3)2杂质的KNO3,可加入过量的K2SO4溶液,过滤,再向滤液中滴加适量的稀硝酸 |
| D、某无色溶液中滴加入盐酸则生成无色气体,该气体能使澄清石灰水变浑浊,则原溶液中一定有CO32- |
下列说法不正确的是( )
| A、元素分析仪可同时对有机物中碳、氢、氧、硫等多种元素进行分析,其特点是样品量少,速度快 |
| B、1H核磁共振谱能反映出有机物中不同环境氢原子的种数和个数 |
| C、根据红外光谱图的分析可以初步判断有机物中具有哪些基团 |
| D、同位素示踪法可以用来确定有机反应中化学键的断裂位置 |
某温度下,反应SO2(g)+
O2(g)?SO3 (g) 的平衡常数K1=100,在同一温度下,反应2SO3(g)?2SO2(g)+O2(g)的平衡常数K2的值为( )
| 1 |
| 2 |
| A、104 |
| B、200 |
| C、10-4 |
| D、10-2 |
胶体区别于其它分散系最本质的特征是( )
| A、外观澄清、稳定 |
| B、丁达尔现象 |
| C、分散至粒子能透过半透膜 |
| D、分散质粒子直径为1---100nm |
关于下列各装置图的叙述中,不正确的是( )
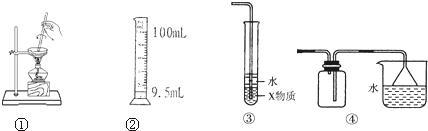

| A、装置①是把饱和食盐水中的食盐提取出来 |
| B、装置②用100mL量筒量取9.5mL液体 |
| C、装置③中X若为CCl4,可用于吸收NH3或HCl,并可防止倒吸 |
| D、装置④可用于收集NH3,并吸收多余的NH3 |
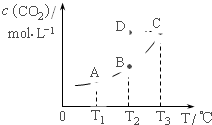 在密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图.下列说法错误的是( )
在密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图.下列说法错误的是( )| A、平衡状态A与C相比,平衡状态A的c(CO)小 |
| B、在T2时,若反应处于状态D,则一定有V正<V逆 |
| C、反应CO(g)+H2O(g)?CO2(g)+H2(g) 的△H>0 |
| D、若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |



