��Ŀ����
6�����ơ�������������Դ�������Ⱦ�Ǹ��ƴ�����������Ҫ���森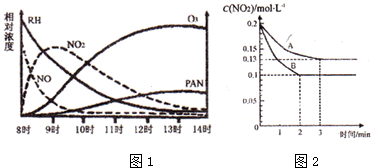
��1���⻯ѧ�����������ɣ�������ʧ������Ҫ�ɷ�ΪRH��������NO��NO2��O3��PAN��CH3COOONO2����ij��������������Щ���ʵ����Ũ�ȱ仯��ͼ1��ʾ�������������������ǣ�������ĸ��
a������8ʱ��ͨ��æ�ڣ��⻯ѧ��������Ҫ�ɷ�ΪRH��NO
b��14ʱ���⻯ѧ��������Ҫ�ɷ�ΪO3��PAN
c��PAN��O3��RH��NOֱ�ӷ�Ӧ����
d��PANֱ����O3ת������
��2����һ�ܱ������з�����Ӧ2NO22NO+O2����Ӧ������NO2��Ũ����ʱ��仯�����������ͼ��ʾ��
��ش�
��������A����Ӧ��ǰ3min��������ƽ����Ӧ����Ϊ����������λ��Ч���֣���
��������A��B�ֱ��ʾ���Ǹ÷�Ӧ��ij��ͬ�����µķ�Ӧ�������B���߸ı�������ǣ��¶ȣ��Ũ�ȡ�����ѹǿ�������¶ȡ�����������
������A��B�ֱ��Ӧ�ķ�Ӧƽ�ⳣ���Ĵ�С��ϵ�ǣ�KA��KB�����������������=����
��3��һ���¶��£���һ�ܱ�������N2O5�ɷ������з�Ӧ��
2N2O5��g��?4NO2��g��+O2��g��I
2NO2��g��?2NO��g��+O2��g��II
��ӦI��ƽ�ⳣ������ʽΪK=$\frac{C{\;}^{4}��NO{\;}_{2}��C��O{\;}_{2}��}{C{\;}^{2}��N{\;}_{2}O{\;}_{5}��}$������ƽ��ʱ��C��NO2��=0.4mol•L-1��C��O2��=1.3mol•L-1����ӦII��NO2��ת����Ϊ80%��N2O5��g������ʼŨ��Ӧ������1mo1•L-1��
���� ��1��a����ͼ1��֪����8ʱ�⻯ѧ��������Ҫ�ɷ�ΪRH��NO��
b����ͼ1��֪14ʱ���⻯ѧ��������Ҫ�ɷ�ΪO3��PAN��
c�����������غ��жϣ�
d��O3��Ũ��һֱ�ڼ��ٲ������Ƿ�Ӧ�
��2���ٸ��ݱ仯��Ũ��֮�ȵ��ڻ�ѧ������֮���Լ���Ӧ���ʹ�ʽv=$\frac{��c}{��t}$�����㣻
����ͼ������A��B�ı仯��֪������B����ƽ��ʱ�������A�̣���Ӧ���ʿ죬ƽ��ʱCD2Ũ�Ƚ�����A�ͣ�ת���ʸߣ�
���ɢڷ�����֪������B���¶ȱ�����A���¶ȸߣ��÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�ƶ���ƽ�ⳣ������
��3��ƽ�ⳣ������ʽK=$\frac{C{\;}^{4}��NO{\;}_{2}��C��O{\;}_{2}��}{C{\;}^{2}��N{\;}_{2}O{\;}_{5}��}$��
�����ӦI�ͷ�ӦII������������Ũ�ȷֱ�ΪXmol•L-1��Y mol•L-1��Ȼ�����ݷ����齨����ϵ��⣬�ó���ӦII��NO2��ת���ʺ�N2O5��g������ʼŨ�ȣ�
��� �⣺��1��a����ͼ1����8ʱ�⻯ѧ��������Ҫ�ɷ�ΪRH��NO����a��ȷ��
b����ͼ1��֪14ʱ���⻯ѧ��������Ҫ�ɷ�ΪO3��PAN����b��ȷ��
c�����������غ��֪����Ԫ���������غ㣬��c����
d��O3��Ũ��һֱ�ڼ��ٲ������Ƿ�Ӧ���d����
��ѡ��ab��
��2������ͼ����A��֪��3min��Ũ��NO2�仯Ϊ0.2mol/L-0.13mol/L=0.07mol/L���ɷ���ʽ��֪��c��D2��=$\frac{1}{2}$��0.07mol/L=0.035mol/L������3min��v��D2��=$\frac{0.035}{3}$=0.0117mol/��L•min�����ʴ�Ϊ��0.0117mol/��L•min����
�ڸ÷�ӦΪ�����С�����ȷ�Ӧ������NO2Ũ�ȣ���Ӧ�ӿ죬��NO2ת���ʽ��ͣ�����ѹǿ����Ӧ�ӿ죬��NO2ת���ʽ��ͣ�ʹ�ô�������Ӧ�ӿ죬ת���ʲ��䣻�����¶ȣ���Ӧ�ӿ죬ƽ��������Ӧ�����ƶ���NO2ת��������Ϊ�����¶ȣ��ʴ�Ϊ���¶ȣ�
���ɢڷ�����֪������B���¶ȱ�����A���¶ȸߣ��÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�ƶ���ƽ�ⳣ������KA��KB���ʴ�Ϊ������
��3��ƽ�ⳣ������ʽK=$\frac{C{\;}^{4}��NO{\;}_{2}��C��O{\;}_{2}��}{C{\;}^{2}��N{\;}_{2}O{\;}_{5}��}$��
2N2O5��g��?4NO2��g��+O2��g��
2X 4Xmol•L-1 Xmol•L-1
2NO2��g��?2NO��g��+O2��g��
2Ymol•L-1 Ymol•L-1
������ϵ��X+Y=1.3��4X-2Y=0.4����ã�X=0.5��Y=0.8��
��ӦII��NO2��ת����Ϊ$\frac{1.6}{2}$��100%=80%��N2O5��g������ʼŨ��Ӧ������1mol•L-1���ʴ�Ϊ��K=$\frac{C{\;}^{4}��NO{\;}_{2}��C��O{\;}_{2}��}{C{\;}^{2}��N{\;}_{2}O{\;}_{5}��}$��80%��1��
���� ������Ҫ�����˻�ѧ��Ӧ���ʡ���ѧƽ���֪ʶ�㣬ƽʱ��������ѧ��������������������ѧ���������⡢��������������

 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д�| A�� | 1gH2��8g O2 | |
| B�� | 1molCO��22.4Lˮ������һ��������ѹ��100�棩 | |
| C�� | 18gˮ�ͱ��ʱ22.4L CO2 | |
| D�� | 3molSO2��2mol SO3 |
| A�� | ����̫���ܡ�ˮ�ܡ����ܡ������ܵ�����Դ | |
| B�� | ��������ú��ʯ�ͺ���Ȼ��������������������������Դ���� | |
| C�� | ������չũ���������������Ľո�ת��Ϊ����Ч����Դ | |
| D�� | ������Դ���ģ�ע����Դ���ظ�ʹ�á���Դ��ѭ������ |
| A�� | ����п�̸ɵ�ر���ͨп�̸ɵ�����ܺã��������Ϳɴ���ʱ�������� | |
| B�� | �����Ӵ����š���ʳ����ڱ����ʳƷ��װ���ڷ���С��������������Ϊ�˸ı䷴Ӧ��ת���ʶ���ȡ�Ĵ�ʩ | |
| C�� | 1kg����֬���ɴ洢Լ32 200kJ������һ����ÿ����1km ��ԼҪ����170kJ ���������ÿ�첽��5km��һ�꣨��365��ƣ������ĵ�֬����Լ��9.6kg | |
| D�� | ����������δ��ʱϴ������Һ�к�NaCl�������ܷ����绯ѧ��ʴ���ɺ��ɫ��� |
 ij��ȤС���ͬѧ����ͼ��ʾװ���о��йص绯ѧ�����⣬���պϸ�װ�õĵ��ʱ���۲쵽������ָ�뷢����ƫת��
ij��ȤС���ͬѧ����ͼ��ʾװ���о��йص绯ѧ�����⣬���պϸ�װ�õĵ��ʱ���۲쵽������ָ�뷢����ƫת�� ���û�ѧ��Ӧԭ������������⣮
���û�ѧ��Ӧԭ������������⣮ ��H=+124kJ•mol-1
��H=+124kJ•mol-1
 ��
��