题目内容
19.某无色溶液中含Na+、I-、NO3-、Cl-,加入下列哪种溶液不会使其变色( )| A. | 酸化的淀粉溶液 | B. | 硫酸钠溶液 | C. | H2O2溶液 | D. | 氯水 |
分析 Na+、I-、NO3-、Cl-可以共存,在酸性条件下I-可以NO3-被氧化为I2,加强氧化性物质也能把I-氧化为I2,生成单质碘,则溶液会变色.
解答 解:A.在酸性条件下I-可以NO3-被氧化为I2,则溶液会变为蓝色,故A不选;
B.加入硫酸钠溶液,与I-不反应,则溶液不变色,故B选;
C.H2O2具有强氧化性,能把I-氧化为I2,则溶液会变色,故C不选;
D.氯水具有强氧化性,能把I-氧化为I2,则溶液会变色,故D不选.
故选B.
点评 本题考查了氧化还原反应、离子共存问题,为高频考点,侧重于学生的分析能力的考查,注意把握常见离子的性质以及离子之间发生的反应,题目难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
9.某物质在空气中燃烧的化学方程式为X+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+2H2O下列说法正确的是( )
| A. | X 的化学式是C2H4 | B. | 该反应属于置换 | ||
| C. | O 2中氧元素的化合价为-2 | D. | CO 2中碳、氧元素的质量比为 1:2 |
14.结合如图判断,下列叙述正确的是( )
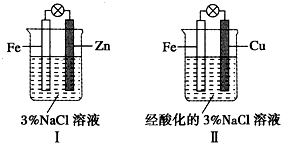

| A. | Ⅰ是验证牺牲阳极的阴极保护法的实验装置 | |
| B. | Ⅰ和Ⅱ中负极反应式均是:Fe-2e-=Fe2+ | |
| C. | Ⅰ和Ⅱ中正极反应式均是:2H++2e-=H2 | |
| D. | Ⅰ和Ⅱ中分别加入少量K3Fe(CN)6溶液,均有蓝色沉淀 |
4.在水溶液中能大量共存的离子组是( )
| A. | K+、Cl-、NO3- | B. | Al3+、OH-、SO42- | C. | H+、Na+、HCO3- | D. | NH4+、Ca2+、CO32- |
8.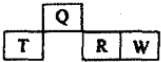 如图是元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是( )
如图是元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是( )
 如图是元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是( )
如图是元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是( )| A. | 气态氢化物的稳定性:W>R | |
| B. | 元素T的最高价氧化物水化物可能是强碱 | |
| C. | Q的原子半径比T小 | |
| D. | W和Q的原子序数相差10 |