题目内容
8.写出下列物质溶于水时的电离方程式:①Fe2(SO4)3Fe2(SO4)3═2Fe3++3SO42-;②NaHSO4NaHSO4═Na++H++SO42-;③KMnO4KMnO4═K++MnO4-.
分析 三种物质都属于盐,都是强电解质,强电解质完全电离,强电解质的电离不可逆,用“═”.
解答 解:①硫酸铁为强电解质,完全电离,电离方程式:Fe2(SO4)3═2Fe3++3SO42-;
②硫酸氢钠为强电解质,完全电离,电离方程式:NaHSO4═Na++H++SO42-;
③高锰酸钾为强电解质,完全电离,电离方程式:KMnO4═K++MnO4-;
故答案为:Fe2(SO4)3═2Fe3++3SO42-;NaHSO4═Na++H++SO42-;KMnO4═K++MnO4-.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱及电离方式是解题关键,注意原子团不能拆,题目难度不大.

练习册系列答案
相关题目
19. 请运用化学反应原理的相关知识研究碳及其化合物的性质.
请运用化学反应原理的相关知识研究碳及其化合物的性质.
(1)在一定体积的密闭容器中,进行如下化学反应,CO2(g)+H2(g)?CO(g)+H2O(g),平衡常数K与温度t℃的关系如下表:
①该反应的化学平衡常数表达式为$\frac{c(CO)×c({H}_{2}O)}{c(C{O}_{2})×c({H}_{2})}$.
②该反应为吸热反应(填“吸热”或“放热”).
③某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(2)工业上一般以CO和H2为原料合成甲醇,一定温度下在恒容容器中,该反应的热化学方程式为:
CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
①下列措施中能说明反应达到平衡状态的是AD.
A.体系压强保持不变
B.混合气体的密度保持不变
C.CO与H2的浓度之比为1:2
D.单位时间内,消耗2molH2的同时消耗1molCH3OH
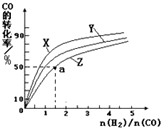
②在恒容容器中合成甲醇,当温度分别为230℃、250℃和270℃时,CO的转化率与n(H2):n(CO)的起始组成比的关系如图所示.已知容器体积1L,起始时CO的物质的量均为1mol.据此判断在上述三种温度中,曲线Z对应的温度是270℃;利用图中a点对应的数据,计算该反应在对应温度下的平衡常数K等于4(mol/L)-2.
 请运用化学反应原理的相关知识研究碳及其化合物的性质.
请运用化学反应原理的相关知识研究碳及其化合物的性质.(1)在一定体积的密闭容器中,进行如下化学反应,CO2(g)+H2(g)?CO(g)+H2O(g),平衡常数K与温度t℃的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
②该反应为吸热反应(填“吸热”或“放热”).
③某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(2)工业上一般以CO和H2为原料合成甲醇,一定温度下在恒容容器中,该反应的热化学方程式为:
CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
①下列措施中能说明反应达到平衡状态的是AD.
A.体系压强保持不变
B.混合气体的密度保持不变
C.CO与H2的浓度之比为1:2
D.单位时间内,消耗2molH2的同时消耗1molCH3OH
②在恒容容器中合成甲醇,当温度分别为230℃、250℃和270℃时,CO的转化率与n(H2):n(CO)的起始组成比的关系如图所示.已知容器体积1L,起始时CO的物质的量均为1mol.据此判断在上述三种温度中,曲线Z对应的温度是270℃;利用图中a点对应的数据,计算该反应在对应温度下的平衡常数K等于4(mol/L)-2.
3.下列物质所属的类别正确的是( )
| A. | 纯碱--盐 | B. | 干冰--混合物 | ||
| C. | 澄清石灰水--纯净物 | D. | 洁净的空气--纯净物 |
13.用ωg氢氧化钠配制一定浓度的溶液来滴定盐酸,若氢氧化钠中混有碳酸钠,则测得盐酸的浓度是( )
| A. | 偏高 | B. | 偏低 | C. | 不变 | D. | 无法判断 |
6.下列热化学方程式或离子方程式中,正确的是( )
| A. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)═2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 氯化镁溶液与氨水反应:Mg2++2NH3•H2O═Mg(OH)2↓+2NH4+ | |
| D. | 氧化铝溶于NaOH溶液:Al2O3+2OH-+3H2O═2Al(OH)3 |

 如图,一密闭气缸被一不漏气可滑动的活塞隔成两部分,左室充有氮气,右室充有混合气体.在室温下将右室的气体点燃,反应后冷却至原室温,活塞最终静止于气缸的某一点(液体体积忽略不计).
如图,一密闭气缸被一不漏气可滑动的活塞隔成两部分,左室充有氮气,右室充有混合气体.在室温下将右室的气体点燃,反应后冷却至原室温,活塞最终静止于气缸的某一点(液体体积忽略不计).