题目内容
下列有关元素周期表、元素周期律的说法中正确的是( )
①所有元素的最高化合价都等于元素原子的最外层电子数
②最外层一个电子的元素一定是金属元素,肯定在元素周期表的第IA族
③ⅡA族中无非金属元素
④第3周期元素随原子序数增大各非金属元素对应的氧化物的水化物酸性一定逐渐增强
⑤同主族元素随原子序数增大,其原子半径逐渐增大
⑥副族元素中没有非金属元素,元素周期表中金属元素的种类比非金属元素多.
①所有元素的最高化合价都等于元素原子的最外层电子数
②最外层一个电子的元素一定是金属元素,肯定在元素周期表的第IA族
③ⅡA族中无非金属元素
④第3周期元素随原子序数增大各非金属元素对应的氧化物的水化物酸性一定逐渐增强
⑤同主族元素随原子序数增大,其原子半径逐渐增大
⑥副族元素中没有非金属元素,元素周期表中金属元素的种类比非金属元素多.
| A、①②③④⑤⑥ | B、①②③⑥ |
| C、③④⑤ | D、③⑤⑥ |
考点:元素周期表的结构及其应用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:①主族元素的最高化合价都等于元素原子的最外层电子数,且O、F没有正极;
②最外层一个电子的元素可能为H,可能为金属元素;
③ⅡA族中为碱土金属元素;
④第3周期元素随原子序数增大各非金属元素对应最高价氧化物的水化物酸性一定逐渐增强;
⑤电子层越多,其原子半径越大;
⑥副族元素中均为金属,元素周期表中100多种元素,金属元素的种类80多种.
②最外层一个电子的元素可能为H,可能为金属元素;
③ⅡA族中为碱土金属元素;
④第3周期元素随原子序数增大各非金属元素对应最高价氧化物的水化物酸性一定逐渐增强;
⑤电子层越多,其原子半径越大;
⑥副族元素中均为金属,元素周期表中100多种元素,金属元素的种类80多种.
解答:
解:①主族元素的最高化合价都等于元素原子的最外层电子数,且O、F没有正极,且过渡元素的最高化合价都不等于元素原子的最外层电子数,故错误;
②最外层一个电子的元素可能为H,可能为金属元素,可能为非金属元素,还可能位于副族,故错误;
③ⅡA族中为碱土金属元素,全为金属元素,故正确;
④第3周期元素随原子序数增大各非金属元素对应最高价氧化物的水化物酸性一定逐渐增强,若不是最高价无此规律,故错误;
⑤同主族元素随原子序数增大,电子层增多,其原子半径逐渐增大,故正确;
⑥副族元素中均为金属,元素周期表中100多种元素,金属元素的种类80多种,则元素周期表中金属元素的种类比非金属元素多,故正确;
故选D.
②最外层一个电子的元素可能为H,可能为金属元素,可能为非金属元素,还可能位于副族,故错误;
③ⅡA族中为碱土金属元素,全为金属元素,故正确;
④第3周期元素随原子序数增大各非金属元素对应最高价氧化物的水化物酸性一定逐渐增强,若不是最高价无此规律,故错误;
⑤同主族元素随原子序数增大,电子层增多,其原子半径逐渐增大,故正确;
⑥副族元素中均为金属,元素周期表中100多种元素,金属元素的种类80多种,则元素周期表中金属元素的种类比非金属元素多,故正确;
故选D.
点评:本题考查元素周期表的结构及应用,为高频考点,把握元素的性质及原子结构与元素位置的关系、元素周期律为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
已知H2(g)+
O2(g)=H2O(g)△H=-241.8kJ/mol,下列说法中不正确的是( )
| 1 |
| 2 |
| A、2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol |
| B、1 mol H2完全燃烧生成液态水放出的热大于241.8kJ |
| C、断裂1mol H2O的化学键吸收的总能量大于断裂1 mol H2和0.5mol O2的化学键所吸收的总能量 |
| D、H2的燃烧热为241.8kJ/mol |
在铜锌电池中,下列叙述正确的是( )
| A、正极附近硫酸根离子浓度增大 |
| B、负极附近硫酸根离子浓度减小 |
| C、正极附近硫酸根离子浓度减小 |
| D、若锌片、铜片同时有气泡冒出,说明锌不纯 |
某烯烃与H2加成后的产物是: ,则该烯烃的结构式可能有( )
,则该烯烃的结构式可能有( )
 ,则该烯烃的结构式可能有( )
,则该烯烃的结构式可能有( )| A、3种 | B、4种 | C、5种 | D、6种 |
下列有关环境问题与NO2无关的是( )
| A、酸雨 | B、温室效应 |
| C、臭氧层空洞 | D、光化学烟雾 |
下列与化学反应能量变化相关的叙述正确的是( )
| A、生成物能量一定低于反应物总能量 |
| B、相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 |
| C、根据盖斯定律,可计算某些难以直接测定的化学反应的反应焓变 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H不同 |
对下列有机反应类型的认识中,不正确的是( )
A、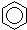 +HNO3 +HNO3
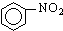 +H2O;取代反应 +H2O;取代反应 | |||
| B、CH4+Cl2→CH3Cl+HCl;置换反应 | |||
C、CH2═CH2+H2O
| |||
D、2CH3CH2OH+O2
|
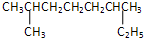 :
: