题目内容
在同温同压下,相同质量的下列气体中体积最大的是( )
| A、O2 |
| B、CH4 |
| C、N2 |
| D、CO2. |
考点:物质的量的相关计算
专题:计算题
分析:同温同压下,相同质量的气体,其体积与摩尔质量成反比,摩尔质量越小,占有的体积越大.
解答:
解:同温同压下,相同质量的气体,其体积与摩尔质量成反比,摩尔质量越小,占有的体积越大.
A、氧气的摩尔质量为32g/mol;
B、甲烷的摩尔质量为16g/mol;
C、氮气的摩尔质量为28g/mol;
D、二氧化碳的摩尔质量为44g/mol,
因此同温同压下,相同质量的气体,甲烷的体积最大,
故选B.
A、氧气的摩尔质量为32g/mol;
B、甲烷的摩尔质量为16g/mol;
C、氮气的摩尔质量为28g/mol;
D、二氧化碳的摩尔质量为44g/mol,
因此同温同压下,相同质量的气体,甲烷的体积最大,
故选B.
点评:本题考查物质的量的有关计算、阿伏伽德罗定律及推论等,比较基础,注意基础知识理解掌握.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
已知热化学方程式:①CO(g)+
O2 (g)=CO2 (g)△H=-283.0kJ?mol-1②H2(g)+
O2(g)=H2O(g);△H=-241.8kJ?mol-1则下列说法正确的是( )

| 1 |
| 2 |
| 1 |
| 2 |

| A、H2的燃烧热为241.8kJ?mol-1 |
| B、根据②推知反应H2(g)+O2 (g)=H2O(l);△H>-241.8kJ?mol-1 |
| C、H2(g)转变成H2O(g)的化学反应一定要释放能量 |
| D、由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.2kJ?mol-1 |
原子序数小于18的元素X,其原子最外层中未成对电子数最多,含这种元素的阴离子可能是( )
| A、XO3- |
| B、XO32- |
| C、XO42- |
| D、XO4- |
不能用Ca2++CO32-=CaCO3↓ 表示离子反应的是( )
| A、CO2通入澄清的石灰水中 |
| B、氯化钙溶液中加入碳酸钾溶液 |
| C、澄清的石灰水与纯碱溶液混合 |
| D、碳酸铵溶液中加入硝酸钙溶液 |
下列说法正确的是( )
| A、铜锌原电池工作时,若有6.5g锌被溶解,电路中就有0.1mol电子通过 |
| B、原电池装置中,电子从正极流向负极 |
| C、可利用CH4和O2的反应设计成原电池 |
| D、在周期表中金属和非金属的分界处易寻找到催化剂和耐高温、耐腐蚀的合金材料 |
萤火虫发光原理如下:

关于荧光素及氧化荧光素的叙述,正确的是( )

关于荧光素及氧化荧光素的叙述,正确的是( )
| A、互为同系物 |
| B、均可发生硝化反应 |
| C、均最多有7个碳原子共平面 |
| D、均可使FeCl3溶液变紫色 |
核糖的结构简式是CH2OH(CHOH)3CHO,它不能发生的反应有( )
| A、酯化 | B、中和 | C、氧化 | D、还原 |
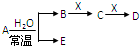 已知A、B、C、D、E、X是H、C、N、O、Na、Al、Cl、Fe等元素组成的常见单质或化合物,它们之间存在如图所示转化关系(部分生成物和反应条件已略去)
已知A、B、C、D、E、X是H、C、N、O、Na、Al、Cl、Fe等元素组成的常见单质或化合物,它们之间存在如图所示转化关系(部分生成物和反应条件已略去)下列说法正确的是( )
| A、若E为氧化物,则X一定为Fe |
| B、若E为氧化物,则在A与水的反应中,氧化剂和还原剂的质量比为1:2 |
| C、若E为单质气体,D为白色沉淀,B可能是共价化合物,也可能是离子化合物 |
| D、若B为单质气体,X可能为C、Na、N2+等 |