题目内容
A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中,A、C及B、D分别是同主族元素;A元素的原子半径是所有主族元素中原子半径最小的;B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍;四种元素所形成的单质中A、B单质是气体,C、D单质是固体.
(1)B、C两元素的名称为:
(2)用电子式表示C2D的形成过程:
 .
.
(3)由B、C两元素所形成的原子个数比为1:1的化合物属于
(4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,其化学方程式为
(1)B、C两元素的名称为:
氧、钠
氧、钠
;(2)用电子式表示C2D的形成过程:


(3)由B、C两元素所形成的原子个数比为1:1的化合物属于
离子
离子
(填“离子”或“共价”)化合物,存在的化学键的种类有离子键、非极性键
离子键、非极性键
,写出它与水反应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑
2Na2O2+2H2O=4Na++4OH-+O2↑
.(4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,其化学方程式为
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.此实验中常加入一种黑色粉未物质,其作用是
| ||
催化剂
催化剂
.分析:A、B、C、D是四种短周期元素,它们的原子序数依次增大,A元素的原子半径是所有主族元素中原子半径最小,则A为氢元素;A、C及B、D分别是同主族元素,B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍,则B、D在在二、三周期,故C处于第三周期,则C为钠元素;B、D分别是同主族元素,B、D两元素的原子核中质子数之和为2(1+11)=24,故B为氧元素,D为硫元素;其中四种元素所形成的单质中A、B单质是气体,C、D单质是固体,符合题意.
解答:解:A、B、C、D是四种短周期元素,它们的原子序数依次增大,A元素的原子半径是所有主族元素中原子半径最小,则A为氢元素;A、C及B、D分别是同主族元素,B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍,则B、D在在二、三周期,故C处于第三周期,则C为钠元素;B、D分别是同主族元素,B、D两元素的原子核中质子数之和为2(1+11)=24,故B为氧元素,D为硫元素;其中四种元素所形成的单质中A、B单质是气体,C、D单质是固体,符合题意.
故A为氢元素,B为氧元素,C为钠元素,D为硫元素;
(1)由上述分析可知,B为氧元素,C为钠元素.
故答案为:氧、钠.
(2)C2D为Na2S,由钠离子与硫离子构成,电子式表示Na2S的形成过程为 .
.
故答案为: .
.
(3)B为氧元素,C为钠元素,由两元素所形成的原子个数比为1:1的化合物为Na2O2,由钠离子与过氧根离子构成,属于离子化合物,钠离子与过氧根离子之间为离子键,过氧根离子中氧原子之间为非极性键;过氧化钠与水反应生成氢氧化钠与氧气,反应离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑.
故答案为:离子;离子键、非极性键;2Na2O2+2H2O=4Na++4OH-+O2↑.
(4)A为氢元素,B为氧元素,两元素所形成的原子个数为1:1的化合物为H2O2,实验室常用H2O2气体O2,反应方程式为2H2O2
2H2O+O2↑,黑色粉未物质二氧化锰其作用是催化剂.
故答案为:2H2O2
2H2O+O2↑;催化剂.
故A为氢元素,B为氧元素,C为钠元素,D为硫元素;
(1)由上述分析可知,B为氧元素,C为钠元素.
故答案为:氧、钠.
(2)C2D为Na2S,由钠离子与硫离子构成,电子式表示Na2S的形成过程为
 .
.故答案为:
 .
.(3)B为氧元素,C为钠元素,由两元素所形成的原子个数比为1:1的化合物为Na2O2,由钠离子与过氧根离子构成,属于离子化合物,钠离子与过氧根离子之间为离子键,过氧根离子中氧原子之间为非极性键;过氧化钠与水反应生成氢氧化钠与氧气,反应离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑.
故答案为:离子;离子键、非极性键;2Na2O2+2H2O=4Na++4OH-+O2↑.
(4)A为氢元素,B为氧元素,两元素所形成的原子个数为1:1的化合物为H2O2,实验室常用H2O2气体O2,反应方程式为2H2O2
| ||
故答案为:2H2O2
| ||
点评:以元素推断为载体,考查学生利用原子的结构来推断元素、常用化学用语等,注意本题中利用A、C与B、D的质子数之和关系分析是解答本题的难点,难度中等.

练习册系列答案
相关题目
a、b、c、d是四种短周期元素.a、b、d同周期,c、d同主族.a的原子结构示意图为 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为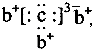 下列比较中正确的是( )
下列比较中正确的是( )
 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为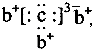 下列比较中正确的是( )
下列比较中正确的是( )| A、原子半径:a>c>d>b | B、最高价含氧酸的酸性c>d>a | C、原子序数:a>d>b>c | D、单质的氧化性a>b>d>c |
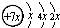 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
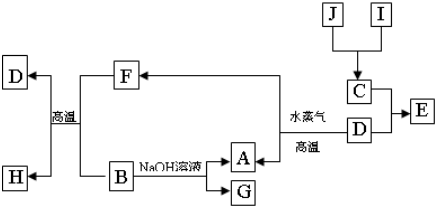
 Al(OH)3+OH-
Al(OH)3+OH-