题目内容
常温下,向0.1mol/L的CH3COOH溶液中加水稀释,下列粒子的浓度减小最快的是( )
| A、CH3COOH |
| B、CH3COO- |
| C、H+ |
| D、OH- |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:加水稀释醋酸能促进醋酸电离,电离方程式中的粒子浓度均减小,由于Kw不变,因此c(OH-)增大.
解答:
解:醋酸溶液中除水分子外还存在CH3COO-、H+、OH-和CH3COOH四中微粒,加水稀释醋酸,电离方程式中的粒子浓度均减小,且能促进醋酸电离,醋酸分子浓度减小最快,由于Kw不变,因此c(OH-)增大,故选A.
点评:本题考查本题考查弱电解质的电离,明确弱电解质电离平衡特点和影响因素是解本题关键,注意醋酸稀释过程中溶液中各离子浓度变化,为易错点.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
下列离子方程式中正确的是( )
| A、石灰石与盐酸反应:CO32-+2H+=CO2↑+H2O |
| B、氢氧化钡与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| C、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| D、碳酸钠与石灰水反应:Ca2++CO32-?=CaCO3↓ |
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是4mol/L和2mol/L,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的混合气体体积为(设反应中HNO3被还原成NO).
| A、448mL |
| B、672mL |
| C、896mL |
| D、224mL |
现有CuO和Fe3O4的混合物7.6g,向其中加入1mol.L-l的H2SO4溶液100mL恰好完全反应,若将15.2g该混合物用足量CO还原,充分反应后剩余固体质量为( )
| A、13.6g |
| B、12g |
| C、6g |
| D、3.2 g |
在0℃和1×105 Pa下,用铂电极电解硫酸铜溶液,当阴极产生6.4g铜时,阳极放出( )
| A、1.12L氧气 |
| B、1.12L氢气 |
| C、2.24L氢气 |
| D、2.24L氧气 |
用水稀释0.1摩/升氨水时,溶液中随着水量的增加而减小的是( )
A、
| ||
B、
| ||
| C、[H+]和[OH-]的乘积 | ||
| D、OH-的物质的量 |
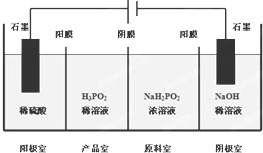 次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性.回答下列问题:
次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性.回答下列问题:
