题目内容
如图所示,a、b、c、d均为石墨电极,通电进行电解。下列说法正确的是( )

A.乙池中d的电极反应为2Cl--2e-=Cl2↑
B.a、c两极产生气体的物质的量相等
C.甲、乙两池中溶液的pH均保持不变
D.乙池中发生的反应为2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
D
【解析】
试题分析:根据装置的连接可知:a、c是阳极,b、d是阴极。A.乙池中d的电极反应为2H++2e-=H2↑,错误;B.在a电极上产生氧气,在c电极上产生氯气,根据整个闭合回路中电子转移数目相等可知在a、c两个电极产生气体的物质的量的比为1:2,不相等,错误;C.甲池中随着电解的进行,溶液由CuSO4逐渐变为H2SO4,、乙池溶液则逐渐由NaCl变为NaOH溶液,所以溶液的pH一个减小,一个增大,错误;D.在乙池中电解饱和NaCl溶液的化学方程式是:2NaCl+2H2O 2NaOH+H2↑+Cl2↑,正确。
2NaOH+H2↑+Cl2↑,正确。
考点:考查电解原理的应用的知识。

(共12分)在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)800 ℃,反应达到平衡时,NO的物质的量浓度是________;升高温度,NO的浓度增大,则该反应是________(填“放热”或“吸热”)反应。
(2)如图中表示NO2的变化的曲线是________。用O2表示从0~2 s内该反应的平均速率v=________。
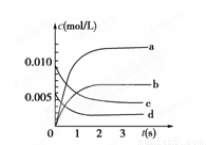
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂

 2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )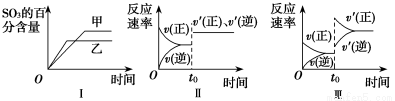
 CO2(g); △H1 C(s)+1/2O2(g)
CO2(g); △H1 C(s)+1/2O2(g) 