��Ŀ����
6��������̼����������ʵ������������ŵ���Ҫ;��֮һ����1��������̼�ĵ���ʽΪ
 ��
����2���������ö�����̼������ķ�Ӧ��ԭ�������ʴ�100%����bd������ţ���
a��CO2+2NH3��������CO��NH2��2+H2O������������
b��CO2+CH4��������CH3COOH
c��CO2+3H2��������CH3OH+H2O
d��
 +nCO2$\stackrel{����}{��}$
+nCO2$\stackrel{����}{��}$
��3����ϡH2SO4�����õ���ɽ�CO2ͬʱת��Ϊ����ȼ�ϣ���ԭ����ͼ��ʾ��

�ٸ�װ������ת���ķ�ʽΪ����ת��Ϊ��ѧ�ܣ�
��һ��ʱ���Cu������Һ�������ӣ�����ӡ������١����䡱����
��ͭ���ϲ�����ϩ�ĵ缫��ӦʽΪ2CO2+12H++12e-=C2H4+4H2O��
��������ֻ����0.17mol CO��0.33mol HCOOH�����·��ת�Ƶ��ӵ����ʵ���Ϊ1mol��
���� ��1��������̼Ϊ���ۻ����������д�������̼��˫����̼ԭ�Ӻ���ԭ�������ﵽ8�����ȶ��ṹ��
��2����ѧ��Ӧ�У�ԭ�ӵ������ʴﵽ100%��Ӧ�Ƿ�Ӧ��ȫ��ת��ΪĿ����û�������������ɣ��Դ˽����⣻
��3����װ�����е�Դ���ǵ���ת��Ϊ��ѧ�ܣ�
��ͭ�缫Ϊ������������Һ��ͭ�缫�����Ƕ�����̼�õ��������ɼ��顢��ϩ�����ᡢһ����̼�ȣ�
�۶�����̼�õ�����������ϩ����ϵ���غ㡢�����غ㡢ԭ���غ���ƽ��д�缫��Ӧ��
��������ֻ����0.17mol CO��0.33mol HCOOH����ϵ缫��Ӧ�������ת��������
��� �⣺��1��������̼�����д�������̼̼˫������ԭ�Ӻ�̼ԭ������㶼Ϊ8�����ӣ�������̼��ȷ�ĵ���ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��2��a���и���Ʒˮ���ɣ�ԭ��������û�дﵽ100%����a����
b����ӦΪ���Ϸ�Ӧ����Ӧ��ȫ��ת��Ϊ�����û�������������ɣ���ԭ�������ʴ�100%����b��ȷ��
c���и�����ˮ���ɣ�ԭ��������û�дﵽ100%����C����
d���÷�ӦΪ�ۺϷ�Ӧ��ԭ�������ʴﵽ100%����d��ȷ��
�ʴ�Ϊ��bd��
��3����װ��ͼ�з�����֪Ϊ���أ���װ������ת���ķ�ʽΪ����ת��Ϊ��ѧ�ܣ�
�ʴ�Ϊ������ת��Ϊ��ѧ�ܣ�
��ͭ�缫Ϊ������������Һ��ͭ�缫�����Ƕ�����̼�õ��������ɼ��顢��ϩ�����ᡢһ����̼�ȣ��缫��������Һ�������ӣ�
�ʴ�Ϊ�����ӣ�
�۶�����̼�õ�����������ϩ����ϵ���غ㡢�����غ㡢ԭ���غ���ƽ��д�缫��ӦΪ��2CO2+12H++12e-=C2H4+4H2O��
�ʴ�Ϊ��2CO2+12H++12e-=C2H4+4H2O��
��������ֻ����0.17mol CO��0.33mol HCOOH��
�缫��ӦΪ��CO2+2e-+2H+=CO+H2O��
2 1
0.34mol 0.17mol
CO2+2e-+2H+=HCOOH
2 1
0.66mol 0.66mol
����ת������=0.34mol+0.66mol=1mol��
�ʴ�Ϊ��1��
���� ���⿼���˷�Ӧ�����������仯��ԭ�������ʡ�����ԭ�����缫��Ӧ��д�ͼ��㣬���ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

| A�� | c��NH4+����ȵģ�NH4��2SO4��NH4HSO4��NH4Cl��Һ�У�c��NH4HSO4����c��c��NH4Cl�� | |
| B�� | ���������Һ�м����������ᣬ�õ������Ի����Һ�У�c��Na+����c��CH3COO-����c��H+����c��OH-�� | |
| C�� | �����ʵ�����NaClO��NaHCO3�����Һ�У�c��HClO��+c��ClO-��=c��HCO3-��+c��H2CO3��+c��CO32-�� | |
| D�� | ij��Ԫ�������ʽ��NaHA��Һ�У�c��H+��+c��Na+��=c��OH-��+c��HA-��+c��A2-�� |
| W | X | |||
| Y | Z |
| A�� | �⻯��е㣺W��Z | |
| B�� | �������Ӧˮ��������ԣ�Y��W | |
| C�� | �����ӵİ뾶��Y��X | |
| D�� | �õ������̬ YZ3 �ķ�����ȡ������ Y |
| A�� | ��ȼ�ͳ���Ϊȼ���������ڼ�����Ⱦ���ŷ� | |
| B�� | ������������ЧԤ��ȣ�ݣ����������ӷ���������˶���� | |
| C�� | ���ࡢ��֬�������ʶ�����C��H��OԪ�� | |
| D�� | �����ʴ�������м�����ʯ�ң��ɶԸ����������� |

| A�� | װ�â�������ʢװ����ŨH2SO4����ˮ | |
| B�� | ʵ��ʱ��Ӧ�ȼ��ȹ�ʽ¯���ٴ�ʢװϡ����ķ�Һ©�� | |
| C�� | Ϊ�����ƵõĹ����Ƿ��������ʣ���Ҫ�õ����Լ�Ϊ���ᡢ˫��ˮ�����軯����Һ | |
| D�� | ��ʵ�����Ʊ�������װ��Ҳ��������������ϡ��Һ���Ȼ�粒��巴Ӧ�Ʊ����� |

���������ӳ�����������������ʽ����ʱ��Һ��pH������
| ������ | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| ��ʼ����ʱ��pH | 1.9 | 7.0 | -- | -- | -- |
| ������ȫʱ��pH | 3.2 | 9.0 | 11.1 | 8 | 9����9�ܽ⣩ |
��2�����˲���ʱ����Ҫ�Գ�������ϴ�ӣ�ϴ������ķ������ز�������©����ע������ˮ�����պý�û�����������ˮ��Ȼ���������ظ�����2��3�Σ�
��3������H2O2������һ����������+3��Crʹ֮ת���+6��Cr��CrO42-��Cr2O72-�����Ա������������ӷ��룺��һ������2Fe2++H2O2+2H+=2Fe3++2H2O�������ӷ���ʽ��ʾ��
��4��������Һ��pH=8��ȥ������������Al3+��Fe3+��
��5�������ӽ�����֬��ԭ��Ϊ��Mn++nNaR��MRn+nNa+��������������������Ca2+��Mg2+��
��6��ͨSO2����ʱ����ԭ���̷������·�Ӧ����дȱ�����ʲ���ƽ����
Na2Cr2O7+3SO2+11H2O=2Cr��OH����H2O��5SO4+1Na2SO4��
 ������Ԫ��W��X��Y��Z��ԭ������������������ZΪ������Z��ԭ������ΪW��2����n��p��q������ЩԪ����ɵĶ�Ԫ����������£�nΪ���壮m��r��s�ֱ���Z��W��X�ĵ��ʣ�t��ˮ��Һ�ʼ�����ɫ��Ӧ�ʻ�ɫ���������ʼ��ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
������Ԫ��W��X��Y��Z��ԭ������������������ZΪ������Z��ԭ������ΪW��2����n��p��q������ЩԪ����ɵĶ�Ԫ����������£�nΪ���壮m��r��s�ֱ���Z��W��X�ĵ��ʣ�t��ˮ��Һ�ʼ�����ɫ��Ӧ�ʻ�ɫ���������ʼ��ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | �����Ӱ뾶��Z��Y��X | |
| B�� | ������P��ֻ�������Ӽ� | |
| C�� | ͼʾת����ϵ�漰�ķ�Ӧ��Ϊ������ԭ��Ӧ | |
| D�� | �����̬�⻯����ȶ��ԣ�W��X |

 �������ǻ����飮
�������ǻ����飮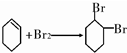 ��
��

 �������E������D������A������ĸ��������װ��E��������i�۲������ͨ�����ʢ���������͵�������ȥ�����е��Ȼ���
�������E������D������A������ĸ��������װ��E��������i�۲������ͨ�����ʢ���������͵�������ȥ�����е��Ȼ���